अध्याय 01 रासायनिक अभिक्रियाएँ और समीकरण
विचार करें इन निम्नलिखित परिस्थितियों को जो हमारे दैनिक जीवन में होती हैं और सोचें कि क्या होता है जब:
- दूध बाएं कमरे के तापमान पर ग्रीष्मकाल के दौरान रखा जाता है।
- एक लोहे का तवा/कड़ाही/कील बाएं अनावृत से नम वायुमंडल में रखी जाती है।
- अंगूर किण्वित हो जाते हैं।
- भोजन पकाया जाता है।
- भोजन हमारे शरीर में पच जाता है।
- हम सांस लेते हैं।
इन सभी उपरोक्त परिस्थितियों में, प्रकृति के ये प्रारंभिक पदार्थ कुछ हद तक बदल जाते हैं। हमने पहले से ही सीखा है भौतिक और रासायनिक परिवर्तनों के बारे में पदार्थों के हमारी पिछली कक्षाओं में। जब भी कोई रासायनिक परिवर्तन घटित होता है, हम कह सकते हैं कि एक रासायनिक प्रतिक्रिया हुई है। तुम शायद सोच रहे होगे कि वास्तव में एक रासायनिक प्रतिक्रिया से क्या अभिप्राय है। हम कैसे जान सकते हैं कि एक रासायनिक प्रतिक्रिया हुई है? आइए कुछ गतिविधियाँ करके इन प्रश्नों के उत्तर खोजें।
गतिविधि 1.1
सावधानी: यह गतिविधि शिक्षक की सहायता से करना आवश्यक है। छात्रों के लिए उपयुक्त चश्मा पहनना बेहतर होगा।
- रेत-काग़ज़ से लगभग 3-4 सेमी लंबे साफ मैग्नीशियम फीते को रगड़ें।
- इसे चिमटे से पकड़ें। इसे आत्मा दीपक या बर्नर से जलाएं और बनने वाली राख को घड़ी-कांच में इकट्ठा करें जैसा कि चित्र 1.1 में दिखाया गया है। मैग्नीशियम फीते को जलाते समय इसे अपनी आंखों से जितना हो सके दूर रखें।
- आप क्या निरीक्षण करते हैं?
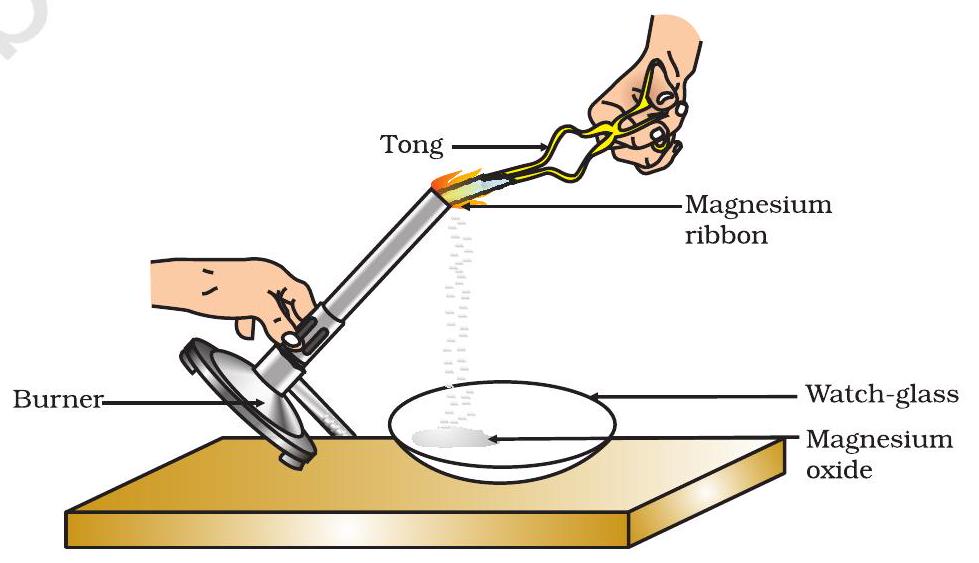
चित्र 1.1 वायु में मैग्नीशियम फीते का जलना और घड़ी-कांच में मैग्नीशियम ऑक्साइड का संग्रह
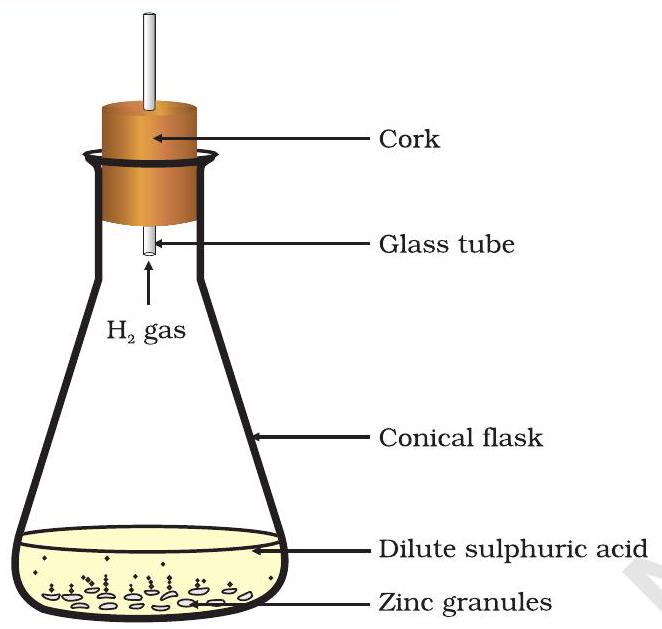
चित्र 1.2 तनुकृत सल्फ्यूरिक अम्ल पर जिंक की क्रिया द्वारा हाइड्रोजन गैस का निर्माण
तुमने देखा होगा कि मैग्नीशियम फीता चमकदार सफेद लौ के साथ जलता है और एक सफेद पाउडर में बदल जाता है। यह पाउडर मैग्नीशियम ऑक्साइड होता है। यह मैग्नीशियम और वायु में मौजूद ऑक्सीजन के बीच प्रतिक्रिया के कारण बनता है।
गतिविधि 1.2
- एक परीक्षण नलिका में सीसा नाइट्रेट का विलयन लो।
- इसमें पोटैशियम आयोडाइड का विलयन डालो।
- तुम क्या निरीक्षण करते हो?
गतिविधि 1.3
- एक शंक्वाकार फ्लास्क या परीक्षण नलिका में कुछ जिंक कणिकाएँ लो।
- इसमें तनुकृत हाइड्रोक्लोरिक अम्ल या सल्फ्यूरिक अम्ल डालो (चित्र 1.2)।
सावधान: इस अम्ल को सावधानी से संभालो।
- क्या तुम जिंक कणिकाओं के आसपास कुछ होते हुए निरीक्षण करते हो?
- इस शंक्वाकार फ्लास्क या परीक्षण नलिका को छुओ। क्या इसके तापमान में कोई परिवर्तन है?
उपरोक्त तीनों गतिविधियों से हम निम्नलिखित प्रेक्षणों के आधार पर कह सकते हैं कि एक रासायनिक प्रतिक्रिया हुई है:
- अवस्था में परिवर्तन
- रंग में परिवर्तन
- गैस का विकास
- तापमान में परिवर्तन
जैसा हम निरीक्षण करते हैं, यह परिवर्तन चारों ओर हमें हो रहा है। हम देख सकते हैं कि हमारे चारों ओर रासायनिक प्रतिक्रियाओं की बड़ी विविधता है। हम इस अध्याय में इन विभिन्न प्रकार की रासायनिक प्रतिक्रियाओं और उनके प्रतीकात्मक प्रतिनिधित्व का अध्ययन करेंगे।
1.1 रासायनिक समीकरण
गतिविधि 1.1 को इस प्रकार वर्णित किया गया है – जब एक मैग्नीशियम फीता ऑक्सीजन में जलाया जाता है, तो यह मैग्नीशियम ऑक्साइड में रूपांतरित हो जाता है। यह विवरण एक रासायनिक प्रतिक्रिया का वाक्य रूप में काफी लंबा है। इसे एक छोटे रूप में लिखा जा सकता है। यह सबसे सरल तरीका है इसे एक शब्द-समीकरण के रूप में लिखना। यह शब्द-समीकरण उपरोक्त प्रतिक्रिया के लिए होगा –
$\underset{(\text{अभिकारक})}{\mathrm{मैग्नीशियम}+\mathrm{ऑक्सीजन}} \rightarrow \underset{(\text{उत्पाद})}{\mathrm{मैग्नीशियम ऑक्साइड}}$
ये पदार्थ जो इस प्रतिक्रिया (1.1) में रासायनिक परिवर्तन से गुजरते हैं, मैग्नीशियम और ऑक्सीजन, अभिकारक हैं। नया पदार्थ मैग्नीशियम ऑक्साइड, जो इस प्रतिक्रिया के दौरान बनाया गया है, उत्पाद है।
एक शब्द-समीकरण परिवर्तन को दर्शाता है जिसमें अभिकारक और उत्पाद के बीच एक तीर लगाया गया है। अभिकारक को बाएँ हाथ की ओर (बायाँ पक्ष) लिखा जाता है और उनके बीच एक जमा चिह्न (+) लगाया जाता है। इसी प्रकार, उत्पाद को दाएँ हाथ की ओर (दाहिना पक्ष) लिखा जाता है और उनके बीच भी एक जमा चिह्न (+) लगाया जाता है। यह तीर उत्पाद की ओर इंगित करता है और प्रतिक्रिया की दिशा को दर्शाता है।
1.1.1 क्या रासायनिक समीकरण लिखने का कोई अन्य संक्षिप्त तरीका है?
रासायनिक समीकरण को अधिक संक्षिप्त और उपयोगी बनाया जा सकता है यदि हम शब्दों के बजाय रासायनिक सूत्रों का उपयोग करें। एक रासायनिक समीकरण एक रासायनिक प्रतिक्रिया का प्रतिनिधित्व करता है। यदि आप मैग्नीशियम, ऑक्सीजन और मैग्नीशियम ऑक्साइड के सूत्रों को याद करें, तो उपरोक्त शब्द-समीकरण को इस प्रकार लिखा जा सकता है:
$$\begin{equation*} \mathrm{Mg} + \mathrm{O}_2 \Rightarrow \mathrm{MgO} \tag{1.2} \end{equation*}$$
गिनती और तुलना करना: यह संख्या परमाणु के प्रत्येक तत्व पर बायाँ पक्ष और दाहिना पक्ष के तीरों से दिखाई देती है। क्या यह संख्या परमाणु के प्रत्येक तत्व पर दोनों भुजाओं पर समान है? यदि हाँ, तो यह समीकरण संतुलित है। यदि नहीं, तो यह समीकरण असंतुलित है क्योंकि द्रव्यमान दोनों भुजाओं पर समान नहीं है। यह एक रासायनिक समीकरण है, एक कंकालीय रासायनिक समीकरण एक प्रतिक्रिया के लिए। समीकरण (1.2) मैग्नीशियम के वायु में जलने का एक कंकालीय रासायनिक समीकरण है।
1.1.2 संतुलित रासायनिक समीकरण
याद करो, द्रव्यमान संरक्षण का नियम तुमने कक्षा नौ में पढ़ा था; द्रव्यमान न तो बनाया जा सकता है और न ही नष्ट किया जा सकता है एक रासायनिक प्रतिक्रिया में। अर्थात्, एक रासायनिक प्रतिक्रिया के उत्पादों में मौजूद कुल द्रव्यमान तत्वों के बराबर होता है जो अभिकारकों में मौजूद थे।
दूसरे शब्दों में, प्रत्येक तत्व के परमाणुओं की संख्या किसी रासायनिक प्रतिक्रिया से पहले और बाद में समान रहती है। इसलिए हमें एक रासायनिक समीकरण को संतुलित करना होता है। क्या यह रासायनिक समीकरण (1.2) संतुलित है? आइए सीखते हैं कि किसी रासायनिक समीकरण को चरणबद्ध तरीके से कैसे संतुलित किया जाता है। यह गतिविधि 1.3 के लिए शब्द-समीकरण इस प्रकार हो सकता है:
[\mathrm{Zinc + Sulphuric\ acid} \rightarrow \mathrm{Zinc\ sulphate + Hydrogen}]
इस उपरोक्त शब्द-समीकरण को निम्नलिखित रासायनिक समीकरण द्वारा प्रस्तुत किया जा सकता है:
[\mathrm{Zn} + \mathrm{H_2SO_4} \rightarrow \mathrm{ZnSO_4} + \mathrm{H_2}]
आइए जांचते हैं कि विभिन्न तत्वों के परमाणुओं की संख्या तीर के दोनों ओर समान है या नहीं।
| तत्व | परमाणुओं की संख्या अभिकारक में (बायाँ पक्ष) | परमाणुओं की संख्या उत्पाद में (दाहिना पक्ष) |
|---|---|---|
| $\mathrm{Zn}$ | 1 | 1 |
| $\mathrm{H}$ | 2 | 2 |
| $\mathrm{S}$ | 1 | 1 |
| $\mathrm{O}$ | 4 | 4 |
जैसा कि संख्या के परमाणु का प्रत्येक तत्व समान होता है, इसलिए दोनों भुजाओं का यह तीर, Eq. (1.3) एक संतुलित रासायनिक समीकरण है। आइए हम इस निम्नलिखित रासायनिक समीकरण को संतुलित करने का प्रयास करें - $$\begin{equation*} \mathrm{Fe} + \mathrm{H}{2}\mathrm{O} \Rightarrow \mathrm{Fe}{3}\mathrm{O}{4} + \mathrm{H}{2} \tag{1.4} \end{equation*}$$
चरण I: रासायनिक समीकरण को संतुलित करने के लिए, पहले प्रत्येक सूत्र के चारों ओर डिब्बे आकर्षित करें। समीकरण को संतुलित करते समय इन डिब्बों के अंदर कुछ भी परिवर्तित न करें। $$\begin{equation*} \mathrm{Fe} + \mathrm{H}{2}\mathrm{O} \Rightarrow \mathrm{Fe}{3}\mathrm{O}{4} + \mathrm{H}{2} \tag{1.5} \end{equation*}$$
चरण II: असंतुलित समीकरण (1.5) में उपस्थित विभिन्न तत्वों के परमाणुओं की संख्या सूचीबद्ध करें।
| तत्व | अभिकारक में परमाणुओं की संख्या (बायाँ पक्ष) | उत्पाद में परमाणुओं की संख्या (दाहिना पक्ष) |
|---|---|---|
| $Fe$ | 1 | 3 |
| $H$ | 2 | 2 |
| $O$ | 1 | 4 |
चरण III: यह अक्सर सुविधाजनक होता है प्रारंभिक संतुलन उस यौगिक से करना जिसमें अधिकतम परमाणुओं की संख्या होती है। यह अभिकारक या उत्पाद दोनों हो सकता है। उस यौगिक में वह तत्व चुनिए जिसमें अधिकतम परमाणुओं की संख्या हो। इन मानदंडों का उपयोग करते हुए, हम Fe₃O₄ चुनते हैं और इसमें ऑक्सीजन तत्व को लेते हैं। दाहिने पक्ष पर चार ऑक्सीजन परमाणु हैं और बाएँ पक्ष पर केवल एक। ऑक्सीजन परमाणुओं को संतुलित करने के लिए -
| ऑक्सीजन परमाणु | अभिकारक में | उत्पाद में |
|---|---|---|
| (i) प्रारंभिक | 1 (H₂O में) | 4 (Fe₃O₄ में) |
| (ii) संतुलित | 1 × 4 | 4 |
इन परमाणुओं की संख्या को समान करते समय यह याद रखना चाहिए कि हम प्रतिक्रिया में शामिल यौगिकों या तत्वों के सूत्र नहीं बदल सकते। उदाहरण के लिए, ऑक्सीजन परमाणुओं को संतुलित करने के लिए हम गुणांक ‘4’ रख सकते हैं जैसे 4H₂O, न कि H₂O₄ या (H₂O)₄। अब यह समीकरण आंशिक रूप से संतुलित हो जाता है -
$$\begin{equation*} \mathrm{Fe} + 4 \mathrm{H_2O} \Rightarrow \mathrm{Fe_3O_4} + \mathrm{H_2} \tag{1.6} \end{equation*}$$ (आंशिक रूप से संतुलित समीकरण)
चरण चतुर्थ: Fe और H परमाणु अभी भी असंतुलित हैं। इनमें से किसी एक तत्व को चुनकर आगे बढ़ें। आइए इस आंशिक रूप से संतुलित समीकरण में हाइड्रोजन परमाणुओं को संतुलित करें। H परमाणुओं की संख्या बराबर करने के लिए दाहिने पक्ष पर हाइड्रोजन अणुओं की संख्या चार कर देते हैं।
| परमाणु | अभिकारक में | उत्पाद में |
|---|---|---|
| (i) प्रारंभिक | 8 (in (4\mathrm{H_2O})) | 2 (in (\mathrm{H_2})) |
| (ii) संतुलन के बाद | 8 | 2 × 4 |
अब समीकरण होगा:
$$\begin{equation*} \mathrm{Fe} + 4 \mathrm{H_2O} \Rightarrow \mathrm{Fe_3O_4} + 4 \mathrm{H_2} \tag{1.7} \end{equation*}$$ (आंशिक रूप से संतुलित समीकरण)
चरण V: जांचें कि उपरोक्त समीकरण में उपरोक्त तीसरा तत्व असंतुलित है या नहीं। आप पाएँगे कि केवल एक तत्व बाएँ से दाएँ संतुलित होना बाकी है, वह है लोहा।
| परमाणु का लोहा | अभिकारक में | उत्पाद में |
|---|---|---|
| (i) प्रारंभिक | 1 (Fe में) | 3 (Fe₃O₄ में) |
| (ii) संतुलन से | 1 × 3 | 3 |
Fe को बराबर करने के लिए हम बाएँ पक्ष पर Fe के तीन परमाणु लेते हैं।
[ \begin{equation*} 3,\mathrm{Fe} + 4,\mathrm{H_2O} \Rightarrow \mathrm{Fe_3O_4} + 4,\mathrm{H_2} \tag{1.8} \end{equation*} ]
चरण VI: अंत में, इस संतुलित समीकरण की सत्यता की जाँच करने के लिए हम समीकरण के दोनों भुजाओं पर प्रत्येक तत्व के परमाणुओं की गिनती करते हैं।
[ \begin{equation*} 3,\mathrm{Fe} + 4,\mathrm{H_2O} \Rightarrow \mathrm{Fe_3O_4} + 4,\mathrm{H_2} \tag{1.9} \end{equation*} ]
(संतुलित समीकरण)
ये संख्याएँ परमाणुओं की संख्या को दर्शाती हैं जो तत्व की दोनों भुजाओं पर समान हैं, जैसा कि समीकरण (1.9) में दिखाया गया है। यह समीकरण अब संतुलित है। इस विधि को रासायनिक समीकरण को संतुलित करने की आज़मा-और-जाँच विधि कहा जाता है, जहाँ हम सबसे छोटे पूर्ण संख्या गुणांकों का उपयोग करके समीकरण को संतुलित करते हैं।
चरण VII: भौतिक अवस्थाओं के प्रतीकों का लेखन
सावधानी से जाँचें कि उपरोक्त संतुलित समीकरण (1.9) क्या हमें अभिकारकों और उत्पादों की भौतिक अवस्थाओं के बारे में कोई जानकारी देता है? नहीं, इस समीकरण में उनकी भौतिक अवस्थाओं के बारे में कोई जानकारी नहीं दी गई है।
एक रासायनिक समीकरण को अधिक जानकारीपूर्ण बनाने के लिए, अभिकारकों और उत्पादों की भौतिक अवस्थाओं को उनके रासायनिक सूत्रों के साथ उल्लेखित किया जाता है। गैसीय, द्रव, जलीय और ठोस अवस्थाओं को क्रमशः (g), (l), (aq) और (s) संकेतों द्वारा प्रस्तुत किया जाता है। यदि कोई अभिकारक या उत्पाद पानी के घोल में उपस्थित होता है, तो इसे जलीय (aq) लिखा जाता है।
इस प्रकार संतुलित समीकरण (1.9) बन जाता है:
$$\begin{equation} 3\ \mathrm{Fe} (s) + 4\ \mathrm{H_2O} (g) \Rightarrow \mathrm{Fe_3O_4} (s) + 4\ \mathrm{H_2} (g) \tag{1.10} \end{equation}$$
नोट कीजिए कि प्रतीक $(g)$ का उपयोग $\mathrm{H_2O}$ के साथ यह दर्शाने के लिए किया गया है कि इस अभिक्रिया में पानी भाप के रूप में उपयोग किया गया है। आमतौर पर भौतिक अवस्थाओं को रासायनिक समीकरण में तभी शामिल किया जाता है जब उन्हें विशिष्ट करना आवश्यक होता है। कभी-कभी अभिक्रिया की शर्तें, जैसे तापमान, दबाव, उत्प्रेरक आदि, जिनमें यह अभिक्रिया होती है, समीकरण में तीर के ऊपर और/या नीचे दर्शाई जाती हैं। उदाहरण के लिए -
$$\mathrm{CO} (g) + 2\ \mathrm{H_2} (g) \xrightarrow{340\ \mathrm{atm}} \mathrm{CH_3OH} (l) \tag{1.11}$$
$$6\mathrm{CO_2} (aq) + 12\mathrm{H_2O} (l) \xrightarrow[\text{क्लोरोफिल}]{\text{सूर्यप्रकाश}} \underset{\text{(ग्लूकोज)}}{\mathrm{C_6H_{12}O_6}} (aq) + 6\mathrm{O_2} (aq) + 6\mathrm{H_2O} (l) \tag{1.12}$$
क्या आपने पहले इस पाठ में दिया गया संतुलन समीकरण (1.2) का उपयोग करना सीखा है?
1.2 प्रकार की रासायनिक प्रतिक्रियाएँ
हमने कक्षा नौ में सीखा था कि एक रासायनिक प्रतिक्रिया में एक तत्व के परमाणु दूसरे तत्व में नहीं बदलते। न ही परमाणु गायब हो जाते हैं या कहीं और प्रकट होते हैं। वास्तव में, रासायनिक प्रतिक्रियाएँ परमाणुओं के बीच बॉन्ड्स के टूटने और बनने से संबंधित होती हैं जिससे नए पदार्थ बनते हैं। आप परमाणुओं के बीच बनने वाले बॉन्ड्स के प्रकारों के बारे में अध्याय 3 और 4 में पढ़ेंगे।
1.2.1 संयोजन प्रतिक्रिया
गतिविधि 1.4
- एक बीकर में थोड़ी मात्रा में कैल्शियम ऑक्साइड या तेज़ नींबू लें।
- इसमें धीरे-धीरे पानी डालें।
- अंजीर 1.3 में दिखाए अनुसार इस बीकर को छूएं।
- क्या आपको तापमान में कोई परिवर्तन महसूस होता है?
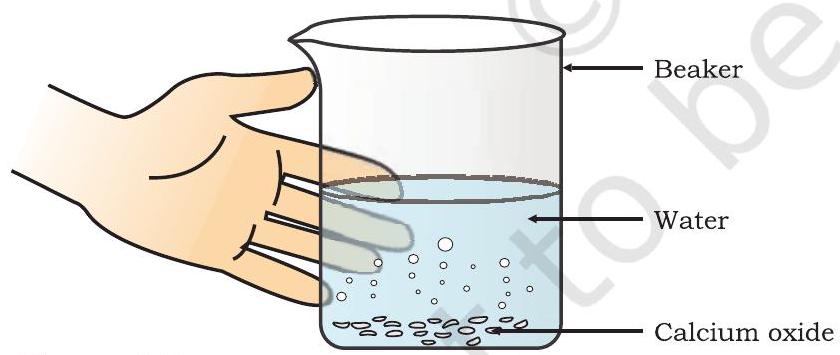
चित्र 1.3 कैल्शियम ऑक्साइड और पानी की इस प्रतिक्रिया से नींबू से भरा हुआ चूना बनता है
कैल्शियम ऑक्साइड प्रबलता से पानी के साथ प्रतिक्रिया करता है और चूने से भरा हुआ नींबू (कैल्शियम हाइड्रॉक्साइड) बनाता है, साथ ही भारी मात्रा में गर्मी उत्सर्जित होती है। $$\ce{CaO(s) + H2O(l) -> Ca(OH)2(aq) + \text{गर्मी}} \tag{1.13}$$ इस प्रतिक्रिया में, कैल्शियम ऑक्साइड और पानी मिलकर एकल उत्पाद, कैल्शियम हाइड्रॉक्साइड बनाते हैं। ऐसी प्रतिक्रिया जिसमें दो या अधिक अभिकारक मिलकर एकल उत्पाद बनाते हैं, संयोजन प्रतिक्रिया कहलाती है।
क्या तुम जानते हो?
इस प्रतिक्रिया 1.13 द्वारा बना चूने से भरा हुआ नींबू का घोल सफेदी दीवारों के लिए उपयोग किया जाता है। कैल्शियम हाइड्रॉक्साइड वायु में उपस्थित कार्बन डाइऑक्साइड के साथ धीरे-धीरे प्रतिक्रिया करता है और दीवारों पर कैल्शियम कार्बोनेट की एक पतली परत बनाता है। कैल्शियम कार्बोनेट दो-तीन दिन बाद बनता है और दीवारों को चमकदार समाप्त प्रदान करता है। यह दिलचस्प है कि यही रासायनिक सूत्र संगमरमर का भी है - $CaCO_3$।
$\underset{\text{(Calcium hydroxide)}}{\mathrm{Ca(OH)_2}}+\mathrm{CO_2(g)} \to \underset{\text{(Calcium carbonate)}}{\mathrm{CaCO_3(s)}} + \mathrm{H_2O(l)} \tag {1.14}$ आइए चर्चा करें कुछ और उदाहरण संयोजन प्रतिक्रियाओं के। (i) कोयले का जलना $$ \begin{equation*} \mathrm{C}(\mathrm{s}) + \mathrm{O}_2(\mathrm{g}) \Rightarrow \mathrm{CO}_2(\mathrm{g}) \tag{1.15} \end{equation*} $$ (ii) पानी का निर्माण $H_2(g)$ और $O_2(g)$ से $$ \begin{equation*} 2\mathrm{H}_2(\mathrm{g}) + \mathrm{O}_2(\mathrm{g}) \Rightarrow 2\mathrm{H}_2\mathrm{O}(\mathrm{l}) \tag{1.16} \end{equation*} $$ सरल भाषा में हम कह सकते हैं कि जब दो या अधिक पदार्थ (तत्व या यौगिक) संयोजित होकर एक एकल उत्पाद बनाते हैं, तो ऐसी प्रतिक्रियाएँ संयोजन प्रतिक्रियाएँ कही जाती हैं।
गतिविधि 1.4 में हमने देखा कि एक बड़ी मात्रा में गर्मी उत्पन्न होती है। यह प्रतिक्रिया मिश्रण को गर्म कर देती है। प्रतिक्रियाएँ जिनमें गर्मी उत्सर्जित होती हैं और साथ-साथ उत्पाद बनते हैं, उष्माक्षेपी रासायनिक प्रतिक्रियाएँ कहलाती हैं। उष्माक्षेपी प्रतिक्रियाओं के अन्य उदाहरण हैं - (i) प्राकृतिक गैस का जलना [\begin{equation*} \mathrm{CH_4(g) + 2O_2(g) \rightarrow CO_2(g) + 2H_2O(g)} \tag{1.17} \end{equation*}] (ii) क्या आप जानते हैं कि श्वसन एक उष्माक्षेपी प्रक्रिया है? हम सभी जानते हैं कि हमें जीवित रहने के लिए ऊर्जा की आवश्यकता होती है। हम इस ऊर्जा को भोजन से प्राप्त करते हैं जो हम खाते हैं। पाचन के दौरान भोजन सरल पदार्थों में टूट जाता है। उदाहरण के लिए, चावल, आलू और रोटी में कार्बोहाइड्रेट्स होते हैं। ये कार्बोहाइड्रेट्स ग्लूकोज बनने के लिए टूट जाते हैं। यह ग्लूकोज हमारे शरीर की कोशिकाओं में ऑक्सीजन के साथ मिलकर ऊर्जा प्रदान करता है। इस प्रतिक्रिया का विशेष नाम श्वसन है, इस प्रक्रिया का अध्ययन आप अध्याय 6 में करेंगे।
$$\begin{equation} \ce{ C6H12O6 (aq) + 6O2 (aq) -> 6CO2 (aq) + 6H2O (l) + \text{ऊर्जा} } \tag{1.18} \end{equation}$$ (iii) सब्ज़ी के पदार्थों के विघटन से कम्पोस्ट बनना भी एक उष्माक्षेपी प्रतिक्रिया का उदाहरण है। गतिविधि 1.1 में दी गई इस प्रतिक्रिया की पहचान कीजिए, जहाँ गर्मी बाहर दी जाती है और एकल उत्पाद का निर्माण होता है। #### 1.2.2 विघटन प्रतिक्रिया > गतिविधि 1.5 » - एक सूखी उबलने वाली नलिका में लगभग 2 g फेरस सल्फेट के क्रिस्टल लीजिए। » - फेरस सल्फेट के क्रिस्टलों का रंग नोट कीजिए। » - उबलने वाली नलिका को बर्नर या आत्मा दीपक की लौ पर इस प्रकार गरम कीजिए जैसा कि चित्र 1.4 में दिखाया गया है। » - गरम करने के बाद क्रिस्टलों के रंग का निरीक्षण कीजिए। 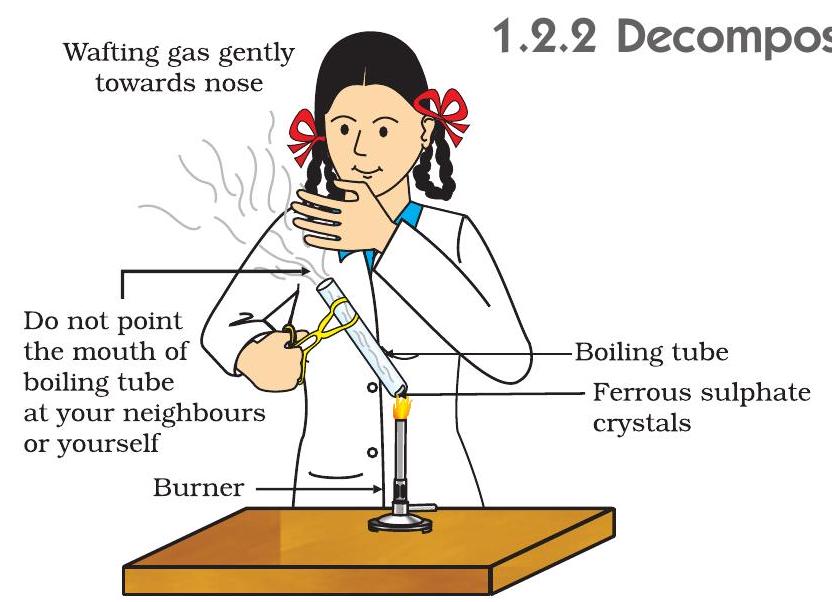 चित्र 1.4 क्रिस्टल युक्त उबलने वाली नलिका को गरम करने का सही तरीका और फेरस सल्फेट की गंध
चित्र 1.4 क्रिस्टल युक्त उबलने वाली नलिका को गरम करने का सही तरीका और फेरस सल्फेट की गंध
क्या तुमने देखा कि यह हरे रंग का फेरस सल्फेट क्रिस्टल बदल गया है? तुम सूंघ सकते हो—इसकी गंध लक्षण गंधक जलने जैसी है।
$$ \ce{ \underset{\text{(फेरस सल्फेट)}}{\ce{FeSO4 (s)}} \xrightarrow[\text{(फेरिक ऑक्साइड)}]{\text{गर्मी}} \underset{\text{Fe}}{\ce{Fe2O3 (s) + SO2 (g) + SO3 (g)}} } \tag{1.19} $$
इस प्रतिक्रिया में तुम निरीक्षण कर सकते हो कि एकल अभिकारक विघटित होकर नीचे से दो सरल उत्पाद बनता है। यह एक विघटन प्रतिक्रिया है। फेरस सल्फेट क्रिस्टल $(\ce{FeSO4.7H2O})$ गरम करने पर पानी खो देता है और इसकी रंगत बदल जाती है। यह फिर विघटित होकर फेरिक ऑक्साइड $(\ce{Fe2O3})$, गंधक डाइऑक्साइड $(\ce{SO2})$ और गंधक ट्राइऑक्साइड $(\ce{SO3})$ बनाता है। फेरिक ऑक्साइड एक ठोस है, जबकि $\ce{SO2}$ और $\ce{SO3}$ गैसें हैं।
विघटन का कैल्शियम कार्बोनेट से कैल्शियम ऑक्साइड और कार्बन डाइऑक्साइड पर गरम करना एक महत्वपूर्ण विघटन प्रतिक्रिया है जिसका उपयोग विभिन्न उद्योगों में किया जाता है। कैल्शियम ऑक्साइड को नींबू या तेज़ नींबू कहा जाता है। इसके बहुत सारे उपयोग हैं - एक इसका उपयोग सीमेंट निर्माण में होता है। जब एक विघटन प्रतिक्रिया को गरम करके बाहर लाया जाता है, तो इसे ऊष्मीय विघटन कहा जाता है। $\underset{\text{ (Limestone) }}{CaCO_3(s)} \stackrel{\text{ Heat }}{\longrightarrow} \underset{\text{ (Quick lime) }}{CaO(s)}+{CO_2(g)} \quad (1.20)$ एक और उदाहरण ऊष्मीय विघटन प्रतिक्रिया का गतिविधि 1.6 में दिया गया है। > गतिविधि 1.6 > > - लगभग 2 g सीसा नाइट्रेट पाउडर को एक उबलना नलिका में लें। > - इस उबलना नलिका को एक चिमटे से पकड़ें और इसे लौ के ऊपर गर्म करें, जैसा कि अंजीर 1.5 में दिखाया गया है। > - आप क्या निरीक्षण करते हैं? इस परिवर्तन को नीचे नोट करें, यदि कोई हो। आप भूरे रंग का धुआँ निकलते हुए देखेंगे। यह धुआँ नाइट्रोजन डाइऑक्साइड $(NO_2)$ का है। यह प्रतिक्रिया इस प्रकार होती है -
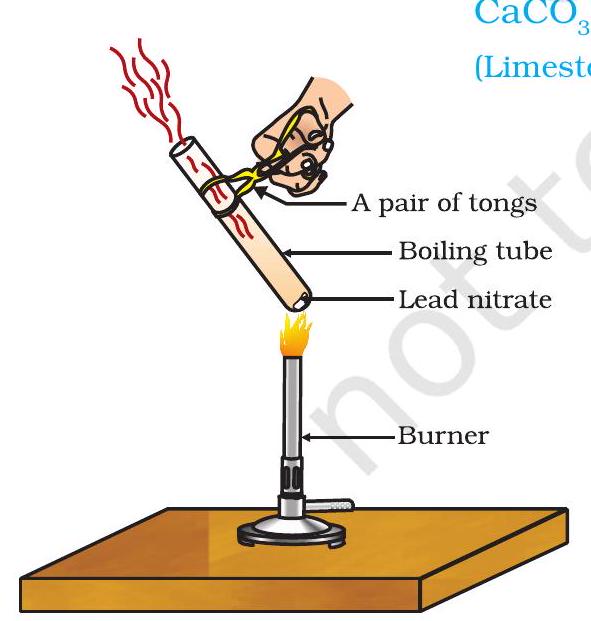 चित्र 1.5 गरम करने पर सीसा नाइट्रेट का विघटन और नाइट्रोजन डाइऑक्साइड का उत्सर्जन $\underset{\text { (Lead nitrate) }}{2 \mathrm{~Pb}\left(\mathrm{NO}_3\right)_2(\mathrm{~s})} \xrightarrow{\text { Heat }} \underset{\text { (Lead oxide) }}{2 \mathrm{PbO}(\mathrm{s})}+\underset{\begin{array}{l}\text { (Nitrogen } \ \text { dioxide) }\end{array}}{4 \mathrm{NO}_2(\mathrm{~g})}+\underset{\text { (Oxygen) }}{\mathrm{O}_2(\mathrm{g})} \quad (1.21)$ आइए हम गतिविधियाँ 1.7 और 1.8 में दी गई कुछ और विघटन प्रतिक्रियाएँ करें।
चित्र 1.5 गरम करने पर सीसा नाइट्रेट का विघटन और नाइट्रोजन डाइऑक्साइड का उत्सर्जन $\underset{\text { (Lead nitrate) }}{2 \mathrm{~Pb}\left(\mathrm{NO}_3\right)_2(\mathrm{~s})} \xrightarrow{\text { Heat }} \underset{\text { (Lead oxide) }}{2 \mathrm{PbO}(\mathrm{s})}+\underset{\begin{array}{l}\text { (Nitrogen } \ \text { dioxide) }\end{array}}{4 \mathrm{NO}_2(\mathrm{~g})}+\underset{\text { (Oxygen) }}{\mathrm{O}_2(\mathrm{g})} \quad (1.21)$ आइए हम गतिविधियाँ 1.7 और 1.8 में दी गई कुछ और विघटन प्रतिक्रियाएँ करें।
गतिविधि 1.7
- एक प्लास्टिक कप लीजिए। इसके आधार पर दो छिद्र करें और इन छिद्रों में रबर रोधक फिट करें। कार्बन इलेक्ट्रोड इन रबर रोधकों में डालें जैसा कि चित्र 1.6 में दिखाया गया है।
- इन इलेक्ट्रोड्स को 6 वोल्ट की बैटरी से जोड़ें।
- इस कप को पानी से भरें इस प्रकार कि इलेक्ट्रोड पानी में डूबे रहें। इस पानी में तनुकृत सल्फ्यूरिक अम्ल की कुछ बूंदें मिलाएं।
- दो परीक्षण नलिकाएँ पानी से भरकर इन दोनों कार्बन इलेक्ट्रोड्स पर उल्टा रखें।
- इस सर्किट को चालू करें और इस उपकरण को कुछ समय के लिए खुला छोड़ दें।
- आप देखेंगे कि दोनों इलेक्ट्रोड्स पर बुलबुले बन रहे हैं। ये बुलबुले परीक्षण नलिकाओं में पानी को विस्थापित कर रहे हैं।
- क्या दोनों परीक्षण नलिकाओं में एकत्रित गैस का आयतन समान है?
- एक बार जब परीक्षण नलिकाएँ संबंधित गैसों से भर जाएं, तो उन्हें ध्यान से हटा लें।
- इन गैसों की जांच एक-एक करके करें - परीक्षण नलिका के मुंह से जलती हुई मोमबत्ती लाकर।
सावधान: यह चरण शिक्षक द्वारा ध्यानपूर्वक करवाया जाना चाहिए।
- प्रत्येक स्थिति में क्या होता है?
- प्रत्येक परीक्षण नलिका में कौन-सी गैस उपस्थित है?
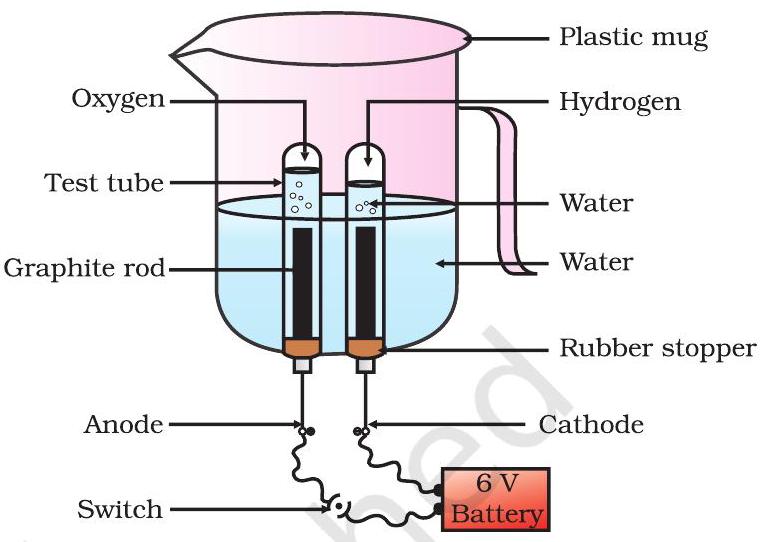 आकृति 1.6 विद्युत अपघटन का पानी
आकृति 1.6 विद्युत अपघटन का पानी
गतिविधि 1.8
- चीन की थाली में लगभग 2 g चाँदी क्लोराइड लें।
- इसका रंग क्या है?
- इस चीन थाली को कुछ समय तक सूर्य के प्रकाश में रखें (आकृति 1.7)।
- कुछ समय बाद चाँदी क्लोराइड के रंग का निरीक्षण करें।
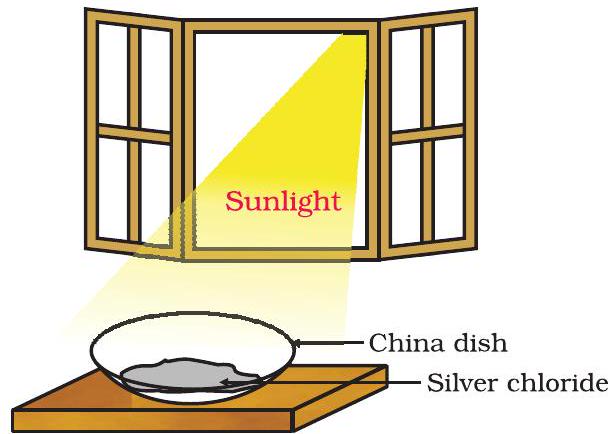 आकृति 1.7 चाँदी क्लोराइध सूर्य के प्रकाश में धूसर हो जाता है और चाँदी धातु तथा क्लोरीन गैस बनाता है। आप देखेंगे कि सफेद चाँदी क्लोराइध सूर्य के प्रकाश में धूसर हो जाता है। इसका कारण प्रकाश द्वारा चाँदी क्लोराइध का चाँदी और क्लोरीन में विघटन है।
आकृति 1.7 चाँदी क्लोराइध सूर्य के प्रकाश में धूसर हो जाता है और चाँदी धातु तथा क्लोरीन गैस बनाता है। आप देखेंगे कि सफेद चाँदी क्लोराइध सूर्य के प्रकाश में धूसर हो जाता है। इसका कारण प्रकाश द्वारा चाँदी क्लोराइध का चाँदी और क्लोरीन में विघटन है।
$$\mathrm{2AgCl (s) \xrightarrow{\text{सूर्य का प्रकाश}} 2Ag (s) + Cl_2 (g)} \tag{1.22}$$
चाँदी ब्रोमाइड भी इसी प्रकार व्यवहार करता है।
$\mathrm{2 AgBr(s) \xrightarrow{\text{ Sunlight }} 2 Ag(s)+Br_2(g)} \quad (1.23)$ यह उपरोक्त प्रतिक्रियाएँ काले और सफेद फोटोग्राफी में उपयोग की जाती हैं। किस रूप की ऊर्जा कारण बनती है इन विघटन प्रतिक्रियाओं का? हमने देखा है कि इन विघटन प्रतिक्रियाओं को आवश्यक ऊर्जा या तो गर्मी, प्रकाश या बिजली के रूप में मिलती है अभिकारकों को तोड़ने के लिए। प्रतिक्रियाएँ जिनमें ऊर्जा अवशोषित होती है, उन्हें उष्माशोषी प्रतिक्रियाएँ कहा जाता है।
लें इस निम्नलिखित गतिविधि को
लीजिए लगभग 2 g बेरियम हाइड्रॉक्साइड एक परीक्षण नलिका में। जोड़िए 1 g अमोनियम क्लोराइड और मिश्रण कीजिए इसे एक कांच की छड़ की सहायता से। छूइए नलिका के निचले भाग को अपनी हथेली से। क्या महसूस करते हैं आप? यह उष्माक्षेपी या उष्माशोषी प्रतिक्रिया है? [[Sc_marker_1]]
1. 2. 3 विस्थापन प्रतिक्रिया
गतिविधि 1.9
- तीन लोहे की कीलें लें और रेत कागज से उन्हें साफ करें।
- दो परीक्षण नलिकाएँ लें और उन्हें (A) और (B) के रूप में चिह्नित करें। प्रत्येक परीक्षण नलिका में लगभग 10 mL तांबा सल्फेट विलयन लें।
- दो लोहे की कीलों को एक धागे से बाँधें और उन्हें ध्यान से परीक्षण नलिका B में तांबा सल्फेट विलयन में लगभग 20 मिनट तक डुबोए रखें [अंजीर. 1.8 (a)]। तुलना के लिए एक लोहे की कील अलग रखें।
- 20 मिनट बाद लोहे की कीलों को तांबा सल्फेट विलयन से बाहर निकालें।
- परीक्षण नलिकाओं (A) और (B) में तांबा सल्फेट विलयन के नीले रंग की तीव्रता की तुलना करें [अंजीर. 1.8 (b)]।
- साथ ही, तांबा सल्फेट विलयन में डुबोई गई लोहे की कील का रंग अलग रखी गई कील से तुलना करें [अंजीर. 1.8 (b)]।
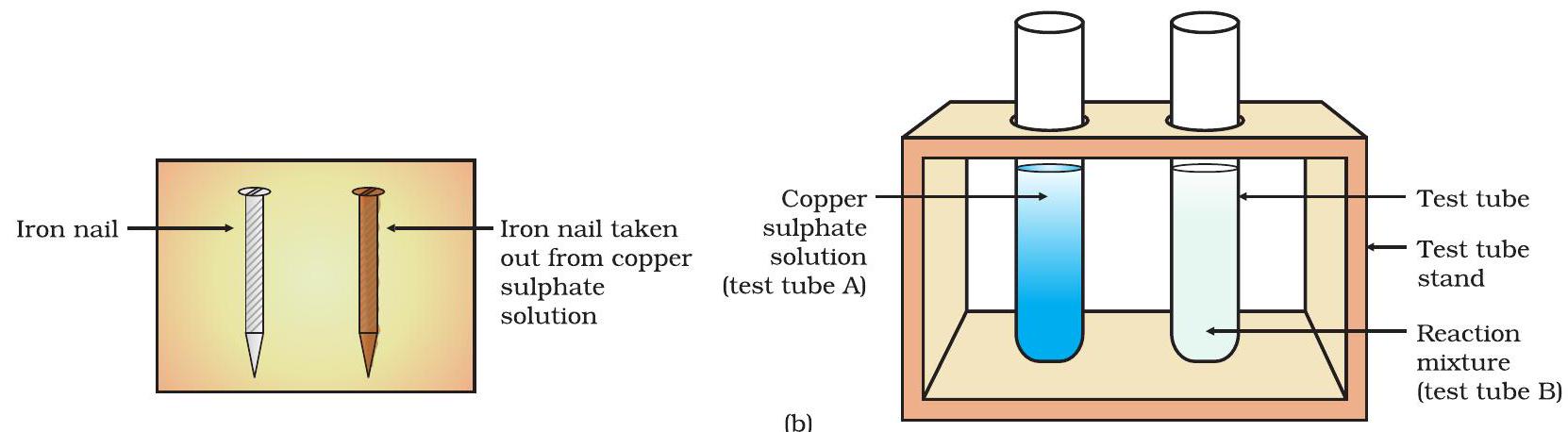 Figure 1.8(b) लोहे की कील और तांबे के सल्फेट घोल की तुलना पहले और बाद में की गई। यह प्रयोग क्यों किया जाता है? लोहे की कील भूरे रंग की हो जाती है और नीले रंग का तांबा सल्फेट घोल फीका पड़ जाता है। यह निम्नलिखित रासायनिक प्रतिक्रिया होती है जिसे यह गतिविधि दर्शाती है - $\mathrm{Fe(s)}+\underset{\text{(Copper sulphate)}}{\mathrm{CuSO_4(aq)}} \rightarrow \underset{\text{Iron sulphate}}{\mathrm{FeSO_4(aq)}}+ \mathrm{Cu(s)} \quad (1.24)$ इस प्रतिक्रिया में, लोहा विस्थापित होता है या हटाया जाता है, अन्य तत्व, तांबा, तांबे के सल्फेट घोल से। यह प्रतिक्रिया विस्थापन प्रतिक्रिया के रूप में जानी जाती है। विस्थापन प्रतिक्रियाओं के अन्य उदाहरण हैं $\mathrm{Zn(s)}+\underset{\text{(Copper sulphate)}}{\mathrm{CuSO_4(aq)}} \rightarrow \underset{\text{Zinc sulphate}}{\mathrm{PbCl_2(aq)}}+ \mathrm{Cu(s)}\quad (1.25)$
Figure 1.8(b) लोहे की कील और तांबे के सल्फेट घोल की तुलना पहले और बाद में की गई। यह प्रयोग क्यों किया जाता है? लोहे की कील भूरे रंग की हो जाती है और नीले रंग का तांबा सल्फेट घोल फीका पड़ जाता है। यह निम्नलिखित रासायनिक प्रतिक्रिया होती है जिसे यह गतिविधि दर्शाती है - $\mathrm{Fe(s)}+\underset{\text{(Copper sulphate)}}{\mathrm{CuSO_4(aq)}} \rightarrow \underset{\text{Iron sulphate}}{\mathrm{FeSO_4(aq)}}+ \mathrm{Cu(s)} \quad (1.24)$ इस प्रतिक्रिया में, लोहा विस्थापित होता है या हटाया जाता है, अन्य तत्व, तांबा, तांबे के सल्फेट घोल से। यह प्रतिक्रिया विस्थापन प्रतिक्रिया के रूप में जानी जाती है। विस्थापन प्रतिक्रियाओं के अन्य उदाहरण हैं $\mathrm{Zn(s)}+\underset{\text{(Copper sulphate)}}{\mathrm{CuSO_4(aq)}} \rightarrow \underset{\text{Zinc sulphate}}{\mathrm{PbCl_2(aq)}}+ \mathrm{Cu(s)}\quad (1.25)$
$\mathrm{Pb(s)}+\underset{\text{(Copper chloride)}}{\mathrm{CuSO_4(aq)}} \rightarrow \underset{\text{Lead sulphate}}{\mathrm{FeSO_4(aq)}}+ \mathrm{Cu(s)}\quad (1.26)$
जिंक और सीसा तांबे से अधिक प्रतिक्रियाशील तत्व हैं। वे तांबे को उसके यौगिक से विस्थापित कर देते हैं।
1.2.4 दोहरा विस्थापन प्रतिक्रिया
गतिविधि 1.10
- एक परीक्षण नलिका में लगभग 3 mL सोडियम सल्फेट का विलयन लें।
- दूसरी परीक्षण नलिका में लगभग 3 mL बेरियम क्लोराइड का विलयन लें।
- इन दोनों विलयनों को मिलाएँ (चित्र 1.9)।
- आप क्या प्रेक्षित करते हैं? आप प्रेक्षित करेंगे कि एक सफेद पदार्थ बनता है, जो पानी में अविलेय है। यह अविलेय पदार्थ एक अवक्षेप के रूप में बनता है। कोई भी प्रतिक्रिया जो अवक्षेप उत्पन्न करती है, वर्षा प्रतिक्रिया कहलाती है।
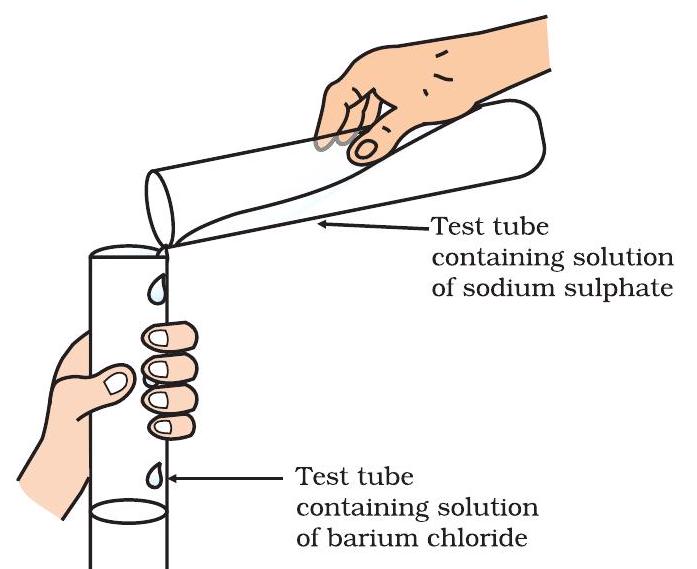
चित्र 1.9 बेरियम सल्फेट और सोडियम क्लोराइड का निर्माण
$ \underset{\text{(Sodium sulphate)}}{\mathrm{Na_2SO_4(aq)}}+\underset{\text{(Barium chloride)}}{\mathrm{BaCl_2(aq)}} \rightarrow \underset{\text{(Barium sulphate)}}{\mathrm{BaSO_4(s)}}+ \underset{\text{(Sodium chloride)}}{\mathrm{2NaCl(aq)}} \quad (1.27)$ इसका क्या कारण है? यह सफेद अवक्षेप $BaSO_4$ है जो इस प्रतिक्रिया में $SO_4^{2-}$ और $Ba^{2+}$ द्वारा बनाया गया है। इसका अन्य उत्पाद सोडियम क्लोराइड है जो इस हल में रहता है। ऐसी प्रतिक्रियाएँ जिनमें अभिकारकों के बीच आयनों का विनिमय होता है, दुगना विस्थापन प्रतिक्रियाएँ कहलाती हैं। > * * याद करना गतिविधि 1 . 2 * * , जहाँ आपने सीसा (II) नाइट्रेट और पोटैशियम आयोडाइड के हल मिश्रित किए थे। > > ( i ) बनाया गया अवक्षेप किस रंग का था? क्या आप इस अवक्षेपित यौगिक का नाम बता सकते हैं? > > ( ii ) इस प्रतिक्रिया के लिए संतुलित रासायनिक समीकरण लिखिए। > > ( iii ) क्या यह भी एक दुगना विस्थापन प्रतिक्रिया है? # # # # 1 . 2 . 5 ऑक्सीकरण और कमी
गतिविधि 1.11
- गर्मी के साथ चीन की थाली में 1 g तांबा पाउडर लीजिए (चित्र 1.10)।
- आप क्या निरीक्षण करते हैं?
- तांबा पाउडर की सतह पर काला तांबा (II) ऑक्साइड की परत बन जाती है।
- यह काला पदार्थ क्यों बनता है?
- ऐसा इसलिए होता है क्योंकि तांबे में ऑक्सीजन मिल जाती है और तांबा ऑक्साइड बन जाता है।
$$\begin{equation} 2 \mathrm{Cu} + \mathrm{O}_{2} \xrightarrow{\text{गर्मी}} 2 \mathrm{CuO} \tag{1.28} \end{equation}$$
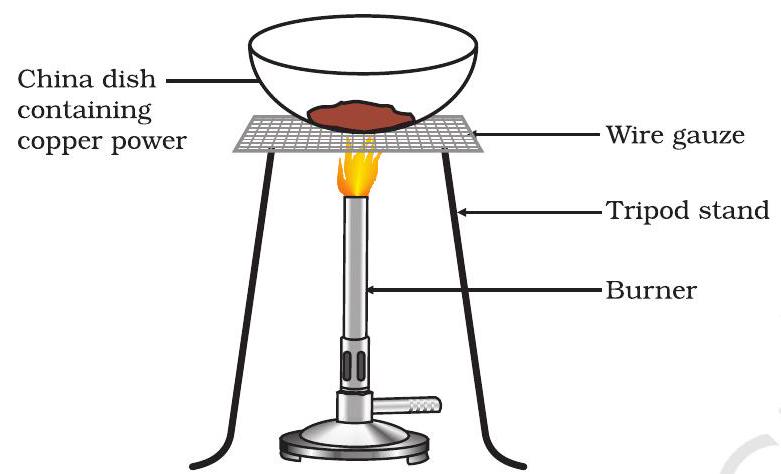
चित्र 1.10 तांबे का ऑक्सीकरण कर तांबा ऑक्साइड बनाना
यदि इस गरम सामग्री $(CuO)$ के ऊपर हाइड्रोजन गैस प्रवाहित की जाए, तो यह सतह पर काला कोटिंग भूरा हो जाता है क्योंकि यह उलट प्रतिक्रिया होती है और तांबा पुनः प्राप्त हो जाता है।
$$\begin{equation} \mathrm{CuO} + \mathrm{H}{2} \xrightarrow{\text{गर्मी}} \mathrm{Cu} + \mathrm{H}{2}\mathrm{O} \tag{1.29} \end{equation}$$
यदि कोई पदार्थ किसी प्रतिक्रिया के दौरान ऑक्सीजन प्राप्त करता है, तो इसे ऑक्सीकृत कहा जाता है। यदि कोई पदार्थ किसी प्रतिक्रिया के दौरान ऑक्सीजन खो देता है, तो इसे कम कहा जाता है। इस प्रतिक्रिया (1.29) के दौरान, यह तांबा (II) ऑक्साइड ऑक्सीजन खोकर कम होता है। यह हाइड्रोजन ऑक्सीजन प्राप्त कर ऑक्सीकृत होता है। दूसरे शब्दों में, एक अभिकारक ऑक्सीकृत होता है जबकि दूसरा कम होता है। ऐसी प्रतिक्रियाओं को ऑक्सीकरण-कमी प्रतिक्रियाएँ या ऑक्सीकरण-अपचयन प्रतिक्रियाएँ कहा जाता है। 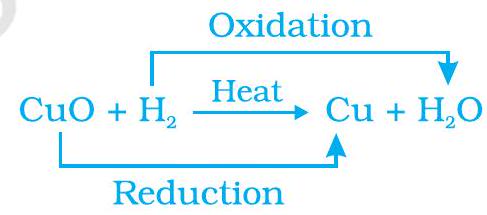 ऑक्सीकरण-अपचयन प्रतिक्रियाओं के कुछ अन्य उदाहरण हैं: $$ \ \mathrm { ZnO + C \rightarrow Zn + CO } \ चतुर्भुज (1.31) $$ $$ \ \mathrm { MnO_2 + 4HCl \rightarrow MnCl_2 + 2H_2O + Cl_2 } \ चतुर्भुज (1.32) $$ प्रतिक्रिया (1.31) में कार्बन CO में ऑक्सीकृत होता है और ZnO Zn में कम होता है। प्रतिक्रिया (1.32) में HCl Cl_2 में ऑक्सीकृत होता है जबकि MnO_2 MnCl_2 में कम होता है।
ऑक्सीकरण-अपचयन प्रतिक्रियाओं के कुछ अन्य उदाहरण हैं: $$ \ \mathrm { ZnO + C \rightarrow Zn + CO } \ चतुर्भुज (1.31) $$ $$ \ \mathrm { MnO_2 + 4HCl \rightarrow MnCl_2 + 2H_2O + Cl_2 } \ चतुर्भुज (1.32) $$ प्रतिक्रिया (1.31) में कार्बन CO में ऑक्सीकृत होता है और ZnO Zn में कम होता है। प्रतिक्रिया (1.32) में HCl Cl_2 में ऑक्सीकृत होता है जबकि MnO_2 MnCl_2 में कम होता है।
उपरोक्त उदाहरण से हम कह सकते हैं कि यदि कोई पदार्थ किसी प्रतिक्रिया के दौरान ऑक्सीजन प्राप्त करता है या हाइड्रोजन खो देता है, तो वह ऑक्सीकृत होता है। यदि कोई पदार्थ ऑक्सीजन खो देता है या हाइड्रोजन प्राप्त करता है, तो वह कम होता है।
याद कीजिए गतिविधि 1.1, जहाँ मैग्नीशियम की फीता हवा (ऑक्सीजन) में चमकती लौ के साथ जलती है और एक सफेद पदार्थ, मैग्नीशियम ऑक्साइड में बदल जाती है। क्या मैग्नीशियम इस प्रतिक्रिया में ऑक्सीकृत होता है या कम होता है?
1.3 क्या तुमने ऑक्सीकरण प्रतिक्रियाओं के प्रभाव को दैनिक जीवन में देखा है?
1.3.1 संक्षारण
क्या तुमने देखा है कि जब लोहा नया होता है तो वह चमकदार होता है, लेकिन जब इसे कुछ समय के लिए छोड़ दिया जाता है तो यह लाल-भूरे रंग के पाउडर से लेपित हो जाता है? इस प्रक्रिया को आमतौर पर लोहे का जंग लगना कहा जाता है। कुछ अन्य धातुएँ भी इस तरह से मलिन हो जाती हैं। क्या तुमने देखा है कि तांबे और चांदी पर बने इस कोटिंग का रंग? जब किसी धातु पर आसपास के पदार्थ जैसे नमी, अम्ल आदि द्वारा हमला होता है, तो इसे संक्षारित करना कहा जाता है और इस प्रक्रिया को संक्षारण कहा जाता है। चांदी पर यह काला कोटिंग और तांबे पर यह हरा कोटिंग संक्षारण के अन्य उदाहरण हैं। संक्षारण कारों के शरीर, पुलों, लोहे की रेलिंगों, जहाजों और सभी धातु से बनी वस्तुओं को नुकसान पहुँचाता है, विशेष रूप से लोहे से बनी वस्तुओं को। लोहे का संक्षारण एक गंभीर समस्या है। प्रत्येक वर्ष क्षतिग्रस्त लोहे को प्रतिस्थापित करने पर विशेष राशि का धन व्यतीत होता है। तुम अध्याय 3 में संक्षारण के बारे में अधिक सीखोगे।
1.3.2 दुर्गन्ध
क्या तुमने कभी मोटे/तेल युक्त भोजन सामग्री को लंबे समय के लिए छोड़ा है?
जब वसा और तेल ऑक्सीकृत होते हैं, तो वे बासी हो जाते हैं और उनकी गंध व स्वाद बदल जाते हैं। आमतौर पर ऐसे पदार्थ जो ऑक्सीकरण को रोकते हैं (प्रतिरक्षक), वसा और तेल युक्त खाद्य पदार्थों में मिलाए जाते हैं। भोजन को हवा से बंद कंटेनर में रखने से ऑक्सीकरण धीमा होता है। क्या तुम जानते हो कि चिप्स निर्माता आमतौर पर चिप्स के साथ बैग्स में नाइट्रोजन जैसी गैस भरते हैं ताकि चिप्स ऑक्सीकृत न हों?
एक पूर्ण रासायनिक समीकरण अभिकारक, उत्पाद और उनके भौतिक राज्यों का प्रतीकात्मक रूप से प्रतिनिधित्व करता है। एक रासायनिक समीकरण संतुलित होता है क्योंकि इसमें प्रत्येक प्रकार के परमाणुओं की संख्या अभिकारक और उत्पाद दोनों भुजाओं पर समान होती है। समीकरण हमेशा संतुलित होना चाहिए।
एक संयोजन प्रतिक्रिया में दो या अधिक पदार्थ मिलकर एक नया एकल पदार्थ बनाते हैं। विघटन प्रतिक्रियाएँ संयोजन प्रतिक्रियाओं के विपरीत होती हैं। एक विघटन प्रतिक्रिया में एक एकल पदार्थ दो या अधिक पदार्थों में विघटित होता है।
प्रतिक्रियाएँ जिनमें गर्मी बाहर दी जाती हैं, उन्हें उष्माक्षेपी प्रतिक्रियाएँ कहा जाता है। प्रतिक्रियाएँ जिनमें ऊर्जा अवशोषित होती है, उन्हें उष्माशोषी प्रतिक्रियाएँ कहा जाता है।
जब एक तत्व दूसरे तत्व के यौगिक से स्वयं को विस्थापित करता है, तो एक विस्थापन प्रतिक्रिया घटित होती है। दोहरे विस्थापन प्रतिक्रियाओं में दो विभिन्न परमाणु या परमाणु समूहों (आयनों) का विनिमय होता है।
वर्षा प्रतिक्रियाएँ अविलेय लवण उत्पन्न करती हैं। प्रतिक्रियाएँ ऑक्सीजन या हाइड्रोजन के लाभ या हानि को भी शामिल कर सकती हैं। ऑक्सीकरण ऑक्सीजन का लाभ या हाइड्रोजन की हानि है। कमी ऑक्सीजन की हानि या हाइड्रोजन का लाभ है।
समूह गतिविधि: निम्नलिखित गतिविधि करें - चार बीकर लें और उन्हें A, B, C और D के रूप में लेबल करें। बीकर A, B और C में 25 mL पानी रखें और बीकर D में तांबा सल्फेट का विलयन रखें। प्रत्येक बीकर में द्रव के तापमान को मापें और अभिलेख करें। बीकर A, B, C और D में क्रमशः दो चम्मच पोटैशियम सल्फेट, अमोनियम नाइट्रेट, अनर्जित तांबा सल्फेट और ठीक लोहा भराव डालें और हिलाएं। अंत में प्रत्येक मिश्रण का तापमान मापें और अभिलेख करें। पता लगाएं कि कौन-सी प्रतिक्रियाएं उष्माक्षेपी और कौन-सी उष्माशोषी हैं।



