अध्याय 03 धातुएँ और अधातुएँ
कक्षा नौ में आपने विभिन्न तत्वों के बारे में सीखा। आपने देखा कि तत्वों को धातु या गैर-धातु के रूप में वर्गीकृत किया जा सकता है, और यह वर्गीकरण उनके गुणधर्मों पर आधारित होता है। सोचिए कि धातुओं और गैर-धातुओं का आपके दैनिक जीवन में क्या उपयोग है। जब आप किसी तत्व को धातु या गैर-धातु के रूप में श्रेणीबद्ध करते हैं, तो आप कौन-से गुणधर्म देखते हैं? ये गुणधर्म उस तत्व के उपयोग से किस प्रकार संबंधित हैं? आइए इन गुणधर्मों को विस्तार से देखें।
3.1 भौतिक गुणधर्म
3.1.1 धातु
पदार्थों को समूहित करने का सबसे आसान तरीका उनके भौतिक गुणधर्मों की तुलना करना है। आइए निम्नलिखित गतिविधियों की सहायता से इसका अध्ययन करें। गतिविधियाँ 3.1 से 3.6 प्रदर्शित करने के लिए, निम्नलिखित धातुओं के नमूने इकट्ठा करें - लोहा, तांबा, एल्यूमिनियम, मैग्नीशियम, सोडियम, सीसा, जिंक और कोई अन्य धातु जो आसानी से उपलब्ध हो।
गतिविधि 3.1
- लीजिए नमूनों को लोहे, तांबे, एल्यूमिनियम और मैग्नीशियम के। नोट कीजिए प्रत्येक नमूने का रूप।
- साफ कीजिए प्रत्येक नमूने की सतह को रेत कागज से मलकर और नोट कीजिए उनका रूप फिर से। धातु, उनके शुद्ध राज्य में, होती है एक चमकती हुई सतह। यह संपत्ति कहलाती है धात्विक चमक।
गतिविधि 3.2
- लीजिए छोटे टुकड़े लोहे, तांबे, एल्यूमिनियम और मैग्नीशियम के। कीजिए कोशिश इन धातुओं को काटने की एक तीक्ष्ण चाकू से और नोट कीजिए आपके प्रेक्षण।
- पकड़िए एक टुकड़ा सोडियम धातु का एक जोड़े से चिमटे के।
सावधान: हमेशा संभालिए सोडियम धातु को ध्यान से। सुखाइए इसे दबाकर फिल्टर कागज की सिलवटों के बीच।
- रखिए इसे एक घड़ी-कांच पर और कीजिए कोशिश इसे काटने की एक चाकू से।
- क्या करते हैं आप निरीक्षण? आप पाएंगे कि धातुएं होती हैं आमतौर पर कठिन। यह कठोरता होती है परिवर्तनशील धातु से धातु।
गतिविधि 3.3
- लोहे, जिंक, सीसे और तांबे के टुकड़े लें।
- इनमें से किसी एक धातु के ब्लॉक को रखें और इसे चार-पाँच बार हथौड़े से पीटें। आप क्या देखते हैं?
- इसे अन्य धातुओं के साथ दोहराएं।
- ध्यान दें कि इन धातुओं की आकृति में क्या बदलाव आता है। आप पाएंगे कि कुछ धातुओं को पतली चादरों में पीटा जा सकता है। इस गुण को नम्यता कहा जाता है। क्या आप जानते हैं कि सोना और चांदी सबसे अधिक नम्य धातुएं हैं?
गतिविधि 3.4
- उन धातुओं की सूची बनाइए जिनके तार आपने दैनिक जीवन में देखे हैं। धातु की यह क्षमता कि उसे पतले तारों में खींचा जा सके, लचीलापन कहलाती है। सोना सबसे अधिक नम्य धातु है। आपको आश्चर्य होगा जानकर कि एक ग्राम सोने से लगभग 2 किलोमीटर लंबा तार खींचा जा सकता है। ऐसा इसलिए है कि इन धातुओं की नम्यता और लचीलेपन के कारण हम इन्हें अपनी आवश्यकताओं के अनुसार विभिन्न आकृतियों में बदल सकते हैं।
क्या तुम जानते हो कि पकाने के बर्तन बनाने के लिए किस धातु का उपयोग किया जाता है? क्या तुम जानना चाहते हो कि ऐसा क्यों किया जाता है? आइए, इसका उत्तर निम्नलिखित गतिविधि से खोजते हैं।
गतिविधि 3.5
- एक एल्यूमिनियम या तांबे का तार लें। इस तार को खड़े ढंग से क्लैंप करें, जैसा कि चित्र 3.1 में दिखाया गया है।
- मोम का उपयोग करके इस तार के मुक्त सिरे पर एक पिन ठीक करें।
- आत्मा दीपक, मोमबत्ती या बर्नर की सहायता से इस तार को गर्म करें, जहाँ यह क्लैंप से पकड़ा गया है।
- कुछ समय बाद तुम क्या देखते हो?
- अपने प्रेक्षणों को नोट करो। क्या यह धातु का तार पिघलता है?
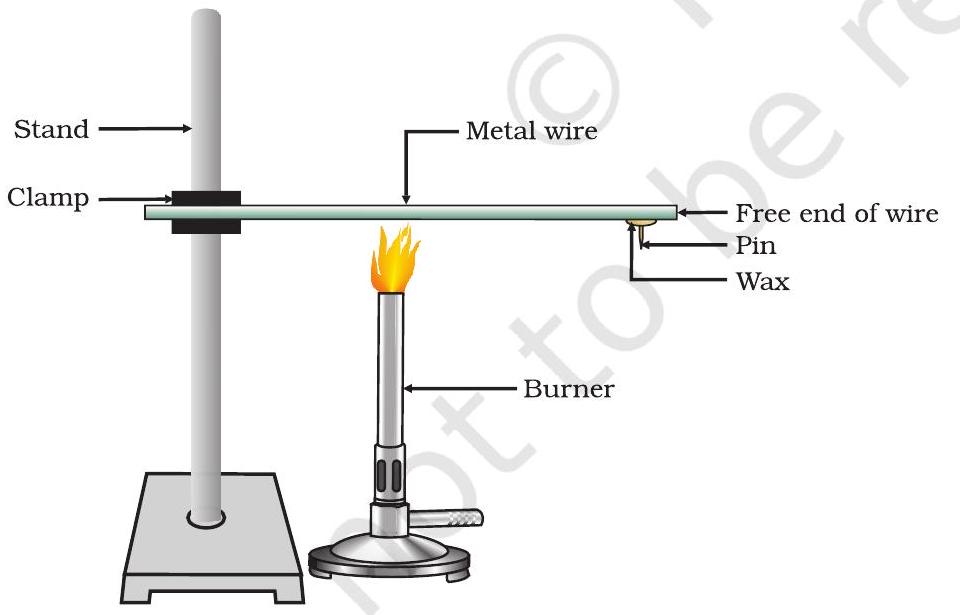
चित्र 3.1 धातु गर्मी का अच्छा चालक होता है। उपरोक्त गतिविधि दिखाती है कि धातु गर्मी का अच्छा चालक होता है और इसका गलनांक ऊँचा होता है। गर्मी के सर्वश्रेष्ठ चालक चांदी और तांबा हैं। सीसा और पारा तुलनात्मक रूप से गर्मी के खराब चालक हैं।
क्या धातु बिजली का आचरण भी करती है? आइए हम पता लगाते हैं।
गतिविधि 3.6
- समुच्चय ऊपर अंजीर 3.2 में दिखाए गए जैसा एक विद्युत सर्किट।
- इस सर्किट के टर्मिनल्स $A$ और $B$ के बीच इस धातु को रखकर परीक्षण करें जैसा दिखाया गया है।
- क्या यह बल्ब चमकता है? यह क्या संकेत देता है?
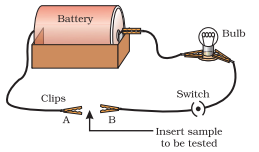
अंजीर 3.2: धातु बिजली का अच्छा चालक होती है। आपने देखा होगा कि तारें जो आपके घर में विद्युत धारा ले जाती हैं, पॉलिविनाइलक्लोराइड (PVC) या रबर जैसी सामग्री की परत से ढकी होती हैं। विद्युत तारों को ऐसे पदार्थ से क्यों लेपित किया जाता है?
जब धातु किसी कठोर सतह से टकराती है तो क्या होता है? क्या वे ध्वनि उत्पन्न करती हैं? जब धातु किसी कठोर सतह से टकराकर ध्वनि उत्पन्न करती है तो इसे स्वरसंगीतमय कहा जाता है। क्या आप अब बता सकते हैं कि विद्यालय की घंटियाँ धातु से क्यों बनाई जाती हैं?
3.1.2 गैर-धातु
मैंने पिछली कक्षा में सीखा था कि वहाँ बहुत-सी धातुओं की तुलना गैर-धातुओं से की गई है। कुछ गैर-धातुओं के उदाहरण हैं—कार्बन, गंधक, आयोडीन, ऑक्सीजन, हाइड्रोजन आदि। ये गैर-धातु या तो ठोस हैं या गैसें हैं, सिवाय ब्रोमीन के जो द्रव है। क्या गैर-धातुओं के भी वही भौतिक गुणधर्म होते हैं जो धातुओं के होते हैं? आइए खोज करें।
गतिविधि 3.7
- कार्बन (कोयला या ग्रेफाइट), गंधक और आयोडीन के नमूने इकट्ठा करें।
- गतिविधियाँ 3.1 से 3.4 और 3.6 इन गैर-धातुओं के साथ करें और अपने प्रेक्षण अभिलेख करें।
- अपने प्रेक्षणों को धातु और गैर-धातु के सन्दर्भ में तालिका 3.1 में संकलित करें।
तालिका 3.1
| तत्व | प्रतीक | सतह का प्रकार | कठोरता | नम्यता | लचीलापन | विद्युत्-चालकता | ध्वनि-वाहकता |
|---|---|---|---|---|---|---|---|
लेकिन इस आधार पर यह प्रेक्षण दर्ज करें कि Table 3.1 में चर्चा की गई सामान्य भौतिक गुणधर्म धातु और गैर-धातु में इस प्रकार के हैं। आपको निष्कर्ष निकालना चाहिए कि हम तत्वों को उनके भौतिक गुणधर्म के आधार पर अकेले समूह नहीं कर सकते, क्योंकि बहुत सारे अपवाद हैं। उदाहरण के लिए - (i) सभी धातुएँ पारे को छोड़कर कमरे के तापमान पर ठोस अवस्था में होती हैं। गतिविधि 3.5 में आपने देखा होगा कि धातुओं का गलन बिंदु ऊँचा होता है, लेकिन गैलियम और सीज़ियम का गलन बिंदु बहुत कम होता है। ये दोनों धातुएँ आपकी हथेली पर रखने पर पिघल जाएँगी। (ii) आयोडीन एक गैर-धातु है लेकिन यह चमकदार होता है। (iii) कार्बन एक गैर-धातु है जो विभिन्न रूपों में मौजूद हो सकता है। प्रत्येक रूप को एक समरूपी रूप कहा जाता है। हीरा, कार्बन का एक समरूपी रूप, सबसे कठिन प्राकृतिक पदार्थ माना जाता है और इसका गलन और उबलना बिंदु बहुत ऊँचा होता है। ग्रेफाइट, कार्बन का एक अन्य समरूपी रूप, बिजली का चालक है।
(चतुर्थ) क्षार धातुएँ (लिथियम, सोडियम, पोटैशियम) नरम होती हैं इसलिए इन्हें चाकू से काटा जा सकता है। इनका घनत्व और गलनांक दोनों कम होते हैं। तत्वों को धातु और अधातु इस आधार पर स्पष्ट रूप से वर्गीकृत किया जा सकता है कि उनके रासायनिक गुणधर्म क्या हैं।
गतिविधि 3.8
- एक मैग्नीशियम फीता और थोड़ा गंधक पाउडर लीजिए।
- मैग्नीशियम फीते को जलाइए। बनी हुई राख को इकट्ठा करके पानी में घोलिए।
- परिणामी विलयन को लाल और नीले दोनों लिटमस कागजों से परखिए।
- क्या मैग्नीशियम के जलने पर बना उत्पाद अम्लीय है या क्षारीय?
- अब गंधक पाउडर को जलाइए। परीक्षण नलिका के ऊपर इस जलते गंधक से निकलने वाले धुएँ को इकट्ठा कीजिए।
- परीक्षण नलिका में थोड़ा पानी डालकर हिलाइए।
- इस विलयन को नीले और लाल दोनों लिटमस कागजों से परखिए।
- क्या गंधक के जलने पर बना उत्पाद अम्लीय है या क्षारीय?
- क्या आप इन प्रतिक्रियाओं के समीकरण लिख सकते हैं?
अधिकांश गैर-धातुएँ जल में घुलने पर अम्लीय ऑक्साइड बनाती हैं, जबकि अधिकांश धातुएँ बुनियादी ऑक्साइड देती हैं। तुम इन धातु ऑक्साइड्स के बारे में अगले खंड में और जानोगे। [[Sc_marker_0]]
3.2 धातुओं के रासायनिक गुणधर्म
हम धातुओं के रासायनिक गुणधर्मों के बारे में अनुभाग 3.2.1 से 3.2.4 तक सीखेंगे। इसके लिए निम्नलिखित धातुओं के नमूने इकट्ठा करो: एल्यूमिनियम, तांबा, लोहा, सीसा, मैग्नीशियम, ज़िंक और सोडियम।
3.2.1 जब धातु को वायु में जलाया जाता है तो क्या होता है?
तुमने गतिविधि 3.8 में देखा होगा कि मैग्नीशियम वायु में चकाचौंध करती हुई सफेद लौ के साथ जलता है। क्या सभी धातुएँ इसी प्रकार प्रतिक्रिया करती हैं? आइए निम्नलिखित गतिविधि करके जाँच करें।
गतिविधि 3.9
सावधानी: निम्नलिखित गतिविधि के लिए शिक्षक की सहायता आवश्यक है। बेहतर होगा यदि छात्र आँखों की सुरक्षा करें।
- उपरोक्त नमूनों में से किसी एक को चिमटे से पकड़ें और लौ पर जलाने का प्रयास करें। इसे अन्य धातु नमूनों के साथ दोहराएं।
- यदि कोई उत्पाद बनता है तो उसे इकट्ठा करें।
- उत्पाद और धातु की सतह को ठंडा होने दें।
- कौन-सी धातु आसानी से जलती है? -जब धातु जल रही थी तो आपने लौ का कौन-सा रंग देखा?
- जलने के बाद धातु की सतह कैसी दिखती है?
- धातुओं को ऑक्सीजन के प्रति उनकी प्रतिक्रियाशीलता के घटते क्रम में व्यवस्थित करें।
- क्या यह उत्पाद पानी में विलेय है?
लगभग सभी धातु ऑक्सीजन के साथ मिलकर धातु ऑक्साइड बनाती हैं।
धातु + ऑक्सीजन → धातु ऑक्साइड
उदाहरण के लिए, जब तांबा हवा में गरम किया जाता है, तो यह ऑक्सीजन के साथ मिलकर तांबा(II) ऑक्साइड बनाता है, जो एक काला ऑक्साइड है।
[\underset{\text{(तांबा)}}{2Cu + O_2} \to \underset{\text{(तांबा(II) ऑक्साइड)}}{2CuO}]
इसी प्रकार, एल्यूमिनियम एल्यूमिनियम ऑक्साइड बनाता है।
$\underset{\text{(Aluminium)}}{4Al}+ 3O_2 \to \underset{\text{(Aluminium oxide)}}{2Al_2O_3}$ याद कीजिए अध्याय 2 से, कैसे तांबा ऑक्साइड प्रतिक्रिया करता है हाइड्रोक्लोरिक अम्ल के साथ। हमने सीखा था कि धातु ऑक्साइड्स प्रकृति में बुनियादी होते हैं। लेकिन कुछ धातु ऑक्साइड्स, जैसे एल्यूमिनियम ऑक्साइड और जिंक ऑक्साइड, दोनों अम्लीय और बुनियादी व्यवहार दिखाते हैं। ऐसे धातु ऑक्साइड्स जो अम्ल और आधार दोनों के साथ प्रतिक्रिया करके लवण और पानी उत्पन्न करते हैं, उभयधर्मी ऑक्साइड्स कहलाते हैं। एल्यूमिनियम ऑक्साइड निम्नलिखित ढंग से अम्ल और आधार दोनों के साथ प्रतिक्रिया करता है - $ Al_2O_3 + 6HCl \to 2AlCl_3 + 3H_2O $ $ Al_2O_3 + 2NaOH \to \underset{\text{(Sodium aluminate)}}{2NaAlO_2} + H_2O $ अधिकांश धातु ऑक्साइड्स पानी में अविलेय होते हैं लेकिन कुछ पानी में विलयन करके क्षार बनाते हैं। सोडियम ऑक्साइड और पोटैशियम ऑक्साइड पानी में विलयन करके निम्नलिखित क्षार उत्पन्न करते हैं - $ \begin{aligned} & Na_2O (s) + H_2O (l) \to 2NaOH (aq) \ & K_2O (s) + H_2O (l) \to 2KOH (aq) \end{aligned} $
हमने देखा है कि गतिविधि 3.9 में सभी धातुएँ ऑक्सीजन के साथ समान दर से प्रतिक्रिया नहीं करती हैं। विभिन्न धातुएँ ऑक्सीजन के प्रति विभिन्न प्रतिक्रियाशीलता दिखाती हैं। धातुएँ जैसे पोटैशियम और सोडियम इतनी प्रबलता से प्रतिक्रिया करते हैं कि वे आग पकड़ लेते हैं यदि खुले में रखे जाएँ। इसलिए, उन्हें सुरक्षित रखने और आकस्मिक आग से बचाने के लिए, इन्हें मिट्टी का तेल या डीजल में डूबा कर रखा जाता है। सामान्य तापमान पर, धातुओं जैसे मैग्नीशियम, एल्यूमिनियम, जिंक, सीसा आदि की सतहें ऑक्साइड की एक पतली परत से ढकी होती हैं। यह सुरक्षात्मक ऑक्साइड परत धातु को आगे ऑक्सीकरण से रोकती है। लोहा गरम करने पर नहीं जलता, लेकिन लोहा प्रबलता से जलता है जब इसे बर्नर की लौ में छिड़का जाता है। तांबा नहीं जलता, लेकिन गरम होने पर इसकी सतह काले रंग के तांबा(II) ऑक्साइड की परत से लेपित हो जाती है। चांदी और सोना ऑक्सीजन के साथ उच्च तापमान पर भी प्रतिक्रिया नहीं करते।
क्या आप जानते हैं?
ऐनोडाइज़िंग एक ऐसी प्रक्रिया है जिसमें एल्यूमिनियम पर मोटी ऑक्साइड परत बनाई जाती है। जब एल्यूमिनियम हवा के संपर्क में आता है, तो इस पर एक पतली ऑक्साइड परत स्वाभाविक रूप से बन जाती है। यह एल्यूमिनियम ऑक्साइड कोट आगे के संक्षारण से बचाता है। इस प्रतिरोध को बढ़ाने के लिए इस ऑक्साइड परत को मोटा बनाया जाता है।
ऐनोडाइज़िंग के दौरान, एक साफ एल्यूमिनियम वस्तु को ऐनोड बनाया जाता है और इसे तनुकृत सल्फ्यूरिक अम्ल में विद्युत-अपघटित किया जाता है। इस प्रक्रिया में ऐनोड पर ऑक्सीजन गैस विकसित होती है जो एल्यूमिनियम के साथ प्रतिक्रिया कर एक मोटी सुरक्षात्मक ऑक्साइड परत बनाती है। इस ऑक्साइड परत को आसानी से रंगा जा सकता है, जिससे दो एल्यूमिनियम वस्तुओं को आकर्षक रूप दिया जा सकता है।
बाद में प्रदर्शन की गई गतिविधि 3.9 में, आपने देखा होगा कि सोडियम सबसे अधिक प्रतिक्रियाशील धातु है। यहाँ इसका नमूना लिया गया है। यह प्रतिक्रिया दर्शाती है कि मैग्नीशियम सोडियम जितना प्रतिक्रियाशील नहीं है। लेकिन जल में ऑक्सीजन की उपस्थिति हमें जिंक, लोहा, तांबा या सीसे की प्रतिक्रियाशीलता के बारे में निर्णय लेने में मदद नहीं करती। आइए इन धातुओं की प्रतिक्रियाशीलता क्रम के बारे में निष्कर्ष पर पहुँचने से पहले कुछ और प्रतिक्रियाएँ देखें।
3.2.2 क्या होता है जब धातु पानी के साथ प्रतिक्रिया करती है?
गतिविधि 3.10
सावधान: यह गतिविधि शिक्षक की सहायता से करें।
- गतिविधि 3.9 में इस्तेमाल किए गए समान धातुओं के नमूने इकट्ठा करें।
- नमूनों के छोटे-छोटे टुकड़े अलग-अलग बीकरों में रखें जो ठंडे पानी से आधे भरे हों।
- कौन-सी धातु ठंडे पानी के साथ प्रतिक्रिया करती है? उन्हें उनकी प्रतिक्रियाशीलता के बढ़ते हुए क्रम में व्यवस्थित करें।
- क्या किसी धातु ने पानी में आग लगाई?
- क्या कोई धातु पहले तैरती है और बाद में डूब जाती है?
- जो धातु ठंडे पानी के साथ प्रतिक्रिया नहीं करती, उसे गरम पानी वाले बीकर में रखें।
- जो धातु गरम पानी के साथ भी प्रतिक्रिया नहीं करती, उसे चित्र 3.3 में दिखाए अनुसार उपकरण में रखें और भाप के साथ उसकी प्रतिक्रिया का निरीक्षण करें।
- कौन-सी धातु भाप के साथ भी प्रतिक्रिया नहीं करती?
- धातुओं को पानी के साथ उनकी प्रतिक्रियाशीलता के घटते हुए क्रम में व्यवस्थित करें।
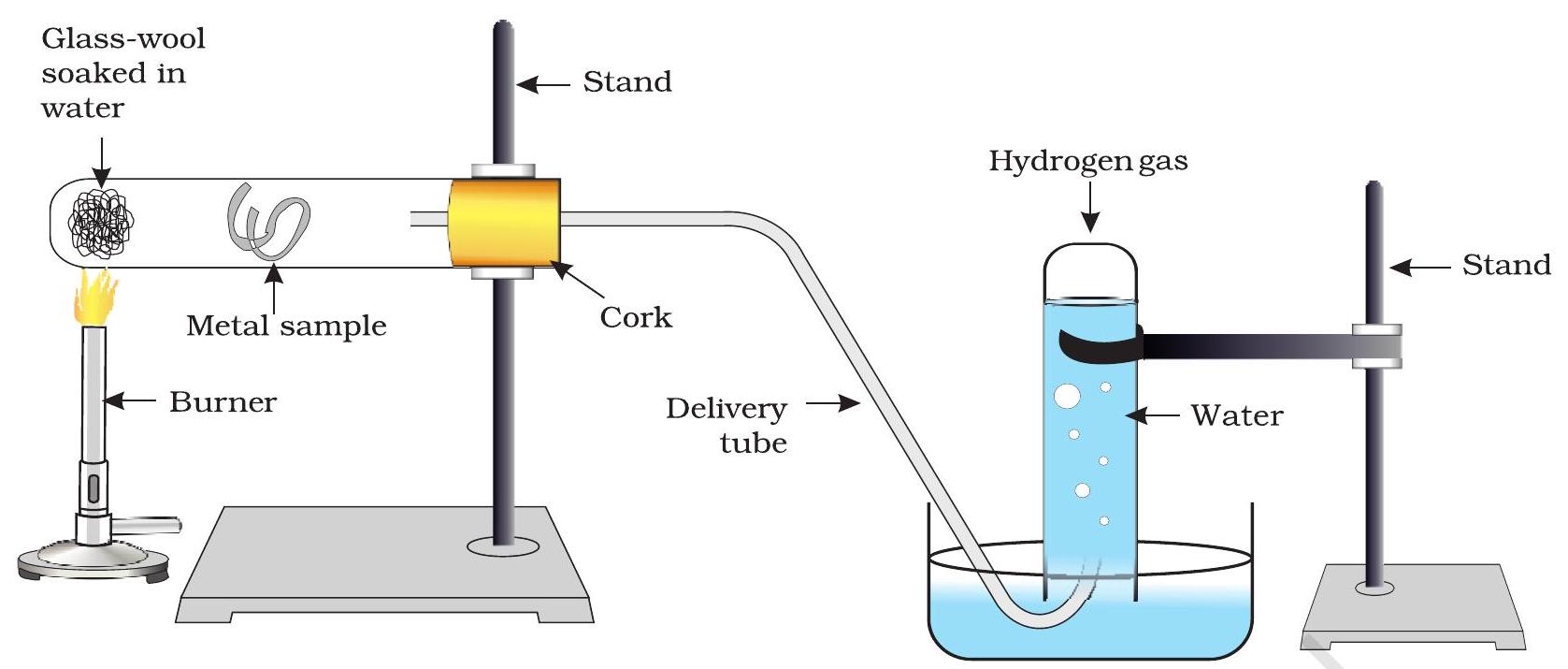
Figure 3.3: क्रिया का भाप पर धातु का पानी के साथ प्रतिक्रिया करना धातु ऑक्साइड और हाइड्रोजन गैस का उत्पादन करता है। धातु ऑक्साइड वे होते हैं जो पानी में विलयन करने पर धातु हाइड्रॉक्साइड बनाते हैं। लेकिन सभी धातुएँ पानी के साथ प्रतिक्रिया नहीं करतीं। धातु + पानी $\rightarrow$ धातु ऑक्साइड + हाइड्रोजन धातु ऑक्साइड + पानी $\rightarrow$ धातु हाइड्रॉक्साइड पोटैशियम और सोडियम जैसी धातुएँ ठंडे पानी के साथ हिंसक रूप से प्रतिक्रिया करती हैं। सोडियम और पोटैशियम के मामले में, यह प्रतिक्रिया इतनी हिंसक और उष्माक्षेपी होती है कि उत्पन्न हाइड्रोजन तुरंत आग पकड़ लेता है।$\begin{aligned} &2K(s) + 2H_2O(l) \rightarrow 2KOH(aq) + H_2(g) + \text{गर्मी ऊर्जा} \ &2Na(s) + 2H_2O(l) \rightarrow 2NaOH(aq) + H_2(g) + \text{गर्मी ऊर्जा} \end{aligned}$कैल्शियम के साथ पानी की यह प्रतिक्रिया कम हिंसक होती है। यह पर्याप्त गर्मी विकसित नहीं करता कि हाइड्रोजन आग पकड़ सके।$Ca(s) + 2H_2O(l) \rightarrow Ca(OH)_2(aq) + H_2(g)$कैल्शियम तैरता हुआ प्रारंभ होता है क्योंकि यह हाइड्रोजन गैस के बुलबुले बनाता है जो धातु की सतह से चिपके रहते हैं।
मैग्नीशियम ठंडे पानी से प्रतिक्रिया नहीं करता। यह गर्म पानी से प्रतिक्रिया करके मैग्नीशियम हाइड्रॉक्साइड और हाइड्रोजन बनाता है। यह तैरता हुआ भी प्रारंभ होता है क्योंकि हाइड्रोजन गैस के बुलबुले इसकी सतह से चिपक जाते हैं। एल्यूमिनियम, लोहा और जिंक जैसी धातुएँ ठंडे या गर्म पानी से प्रतिक्रिया नहीं करतीं, लेकिन ये भाप से प्रतिक्रिया करके धातु ऑक्साइड और हाइड्रोजन बनाती हैं। $ \begin{aligned} &2Al(s) + 3H_2O(g) \rightarrow Al_2O_3(s) + 3H_2(g) \ &3Fe(s) + 4H_2O(g) \rightarrow Fe_3O_4(s) + 4H_2(g) \end{aligned} $ सीसा, तांबा, चांदी और सोना जैसी धातुएँ पानी से बिल्कुल भी प्रतिक्रिया नहीं करतीं।
3.2.3 क्या होता है जब धातु अम्ल से प्रतिक्रिया करती है?
आपने पहले सीखा है कि धातु अम्ल से प्रतिक्रिया करके एक नमक और हाइड्रोजन गैस बनाती है। धातु + तनुकृत अम्ल $\rightarrow$ नमक + हाइड्रोजन क्या सभी धातुएँ इसी प्रकार प्रतिक्रिया करती हैं? आइए जानते हैं।
गतिविधि 3.11
-
इकट्ठा करें सभी धातु नमूने, सोडियम और पोटैशियम को छोड़कर। यदि नमूने मलिन हैं, तो रगड़कर साफ करें रेत कागज से।
सावधान: सोडियम और पोटैशियम को न लें, क्योंकि ये ठंडे पानी के साथ प्रबलता से प्रतिक्रिया करते हैं। -
रखें इन नमूनों को अलग-अलग परीक्षण नलिकाओं में, जिनमें तनुकृत हाइड्रोक्लोरिक अम्ल हो।
-
डुबो दें थर्मामीटर को इन परीक्षण नलिकाओं में, ताकि उसका बल्ब अम्ल में डूबा रहे।
-
ध्यान से निरीक्षण करें बुलबुले बनने की दर।
-
कौन-सी धातु ने प्रबलता से तनुकृत हाइड्रोक्लोरिक अम्ल के साथ प्रतिक्रिया दी?
-
किस धातु के साथ आपने सबसे ऊँचा तापमान अभिलेख किया?
-
व्यवस्थित करें इन धातुओं को प्रतिक्रियाशीलता के घटते क्रम में, तनुकृत अम्ल के साथ।
लिखें समीकरण इन प्रतिक्रियाओं के लिए: मैग्नीशियम, एल्यूमिनियम, जिंक और लोहा — तनुकृत हाइड्रोक्लोरिक अम्ल के साथ।
हाइड्रोजन गैस नहीं विकसित होती जब कोई धातु नाइट्रिक अम्ल के साथ प्रतिक्रिया करता है। ऐसा इसलिए है क्योंकि $HNO_3$ एक प्रबल ऑक्सीकृत करने वाला एजेंट है। यह $H_2$ को पानी से ऑक्सीकृत कर देता है और स्वयं किसी न किसी नाइट्रोजन ऑक्साइड ($N_2O$, $NO$, $NO_2$) में परिवर्तित हो जाता है। परंतु मैग्नीशियम $(Mg)$ और मैंगनीज $(Mn)$ बहुत तनुकृत $HNO_3$ के साथ प्रतिक्रिया करके $H_2$ गैस विकसित करते हैं। आपने क्रियाकलाप 3.11 में देखा होगा कि बुलबुले बनने की दर मैग्नीशियम के मामले में सबसे तेज़ थी। यह प्रतिक्रिया इस मामले में सबसे अधिक उष्माक्षेपी भी थी। प्रतिक्रियाशीलता का क्रम है $Mg>Al>Zn>Fe$। तांबे के मामले में कोई बुलबुले नहीं दिखे और तापमान भी अपरिवर्तित रहा। इससे पता चलता है कि तांबा तनुकृत $HCl$ के साथ प्रतिक्रिया नहीं करता।
क्या आप जानते हैं?
जल राजा (लैटिन में ‘राजसी पानी’) ताज़ा तैयार किया गया सांद्रित हाइड्रोक्लोरिक अम्ल और सांद्रित नाइट्रिक अम्ल का 3:1 अनुपात में मिश्रण है। यह विलयन सोने को घोल सकता है, यद्यपि इनमें से कोई भी अम्ल अकेले ऐसा नहीं कर सकता। जल राजा एक अत्यधिक संक्षारक, धूम्रित द्रव है। यह एक ऐसा अभिकर्मक है जो सोने और प्लैटिनम को घोलने में सक्षम है।
3.2.4 धातुएँ अन्य धातु लवणों के विलयन के साथ कैसे प्रतिक्रिया करती हैं?
गतिविधि 3.12
- लीजिए एक साफ तांबे का तार और एक लोहे की कील।
- रखिए इस तांबे के तार में एक हल का लोहा सल्फेट और इस लोहे की कील में एक हल का तांबा सल्फेट लिया गया है, परीक्षण नलिकाओं में (अंजीर. 3.4)।
- अभिलेख कीजिए आपके प्रेक्षण बाद में 20 मिनट।
- में जो परीक्षण नलिका आपने की, वहाँ आपने क्या प्रतिक्रिया घटित हुई?
- पर क्या आधार पर आप कह सकते हैं कि वह प्रतिक्रिया वास्तव में हुई है?
- क्या आप संबंधित कर सकते हैं आपके प्रेक्षण को इस गतिविधियों 3.9, 3.10 और 3.11 से?
- लिखिए एक संतुलित रासायनिक समीकरण इस प्रतिक्रिया के लिए जो हुई है।
- नाम कीजिए इस प्रकार की प्रतिक्रिया।
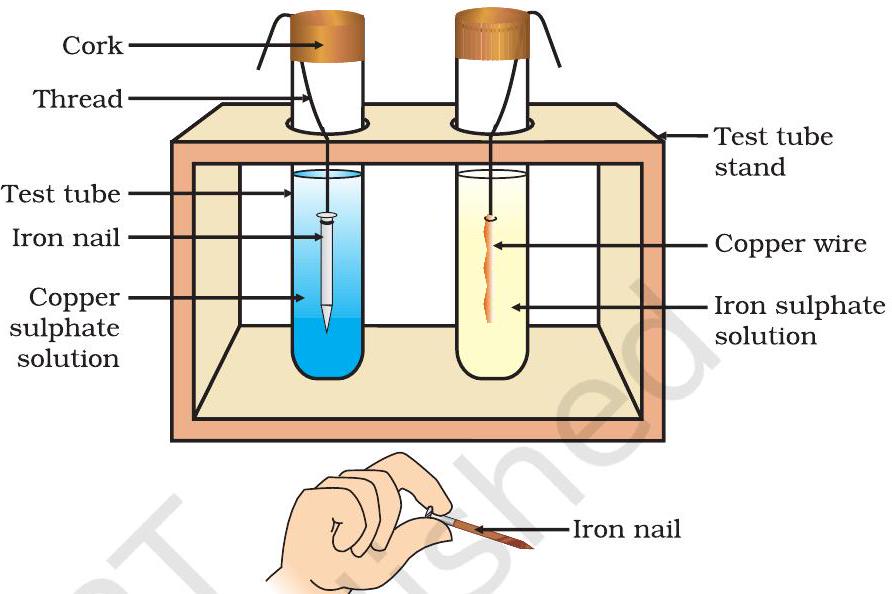
चित्र 3.4 प्रतिक्रिया धातु के साथ नमक हल में - प्रतिक्रियाशील धातु विस्थापित कर सकती है कम प्रतिक्रियाशील धातु को उसके यौगिक से हल या गलित रूप में।
हमने देखा है कि पिछले अनुभाग में सभी धातुएँ समान रूप से प्रतिक्रियाशील नहीं हैं। हमने जाँच की है कि विभिन्न धातुएँ ऑक्सीजन, पानी और अम्ल के साथ कितनी प्रतिक्रियाशील हैं। लेकिन सभी धातुएँ इन अभिकर्मकों के साथ प्रतिक्रिया नहीं करती हैं। इसलिए हम इन सभी धातु नमूनों को उनकी प्रतिक्रियाशीलता के घटते क्रम में रखने में सक्षम नहीं थे। विस्थापन प्रतिक्रियाओं का अध्ययन अध्याय 1 में धातुओं की इस प्रतिक्रियाशीलता के बारे में दो बेहतर प्रमाण देता है। यह सरल और आसान है - यदि धातु A धातु B के हल से विस्थापित करती है, तो यह B से अधिक प्रतिक्रियाशील है।
[\text{धातु A} + \text{नमक हल का B} \rightarrow \text{नमक हल का A} + \text{धातु B}]
तांबा और लोहा में से कौन-सी धातु गतिविधि 3.12 के आपके प्रेक्षण के अनुसार अधिक प्रतिक्रियाशील है?
3.2.5 यह प्रतिक्रियाशीलता श्रृंखला
यह प्रतिक्रियाशीलता श्रृंखला है जो धातुओं की सूची को उनकी घटती हुई गतिविधियों के क्रम में व्यवस्थित करती है। बाद में प्रदर्शित विस्थापन प्रयोगों (गतिविधियाँ 1.9 और 3.12) के आधार पर, निम्नलिखित श्रृंखला (Table 3.2) विकसित की गई है जिसे प्रतिक्रियाशीलता या गतिविधि श्रृंखला कहा जाता है।
Table 3.2 गतिविधि श्रृंखला: धातुओं की सापेक्ष प्रतिक्रियाशीलताएँ
| K | पोटैशियम | $\downarrow$ अधिकांश प्रतिक्रियाशील | | $Na$ | सोडियम | | | $Ca$ | कैल्शियम | | | मि.ग्रा. | मैग्नीशियम | | | अल | एल्यूमिनियम | | | $Zn$ | जिंक | $\downarrow$ प्रतिक्रियाशीलता कम होती है | | $Fe$ | लोहा | | | $Pb$ | सीसा | | | $[H]$ | [हाइड्रोजन] | | | $Cu$ | तांबा | | | $Hg$ | पारा | | | $Ag$ | चांदी | | | $Au$ | सोना | $\downarrow$ न्यूनतम प्रतिक्रियाशील |
[[Sc_marker_1]]
3.3 धातु और गैर-धातु कैसे प्रतिक्रिया देते हैं?
मैंने ऊपर जो गतिविधियाँ दिखाई हैं, वे धातुओं की प्रतिक्रियाएँ हैं जिनमें एक संख्या अभिकर्मक के रूप में कार्य करती है। धातुएँ प्रतिक्रिया देती समय ऐसा क्यों व्यवहार करती हैं? आइए याद करें कि हमने कक्षा नौ में तत्वों के इलेक्ट्रॉनिक विन्यास के बारे में क्या सीखा था। हमने सीखा था कि उत्कृष्ट गैसें, जिनकी संयोजकता कोश पूरी तरह भरी होती है, बहुत कम रासायनिक गतिविधि दिखाती हैं। हमने यह भी समझाया कि तत्वों की यह प्रतिक्रियाशीलता इस प्रवृत्ति से उत्पन्न होती है कि वे पूरी तरह भरी हुई संयोजकता कोश प्राप्त करना चाहते हैं। आइए उत्कृष्ट गैसों और कुछ धातुओं व अधातुओं के इलेक्ट्रॉनिक विन्यास पर एक नज़र डालें।
हम देख सकते हैं कि Table 3.3 में सोडियम परमाणु के बाहरीतम शेल में एक इलेक्ट्रॉन है। यदि यह इलेक्ट्रॉन खो देता है, तो इसका M शेल खाली हो जाता है और L शेल अब इसका बाहरीतम शेल बन जाता है, जो एक स्थिर अष्टक है। इस परमाणु के नाभिक में अभी भी 11 प्रोटॉन हैं, लेकिन इलेक्ट्रॉनों की संख्या 10 हो जाती है, इसलिए इसमें एक नेट सकारात्मक आवेश होता है, जिससे हमें सोडियम धनायन Na⁺ मिलता है। दूसरी ओर, क्लोरीन के बाहरीतम शेल में सात इलेक्ट्रॉन हैं और इसे अपना अष्टक पूरा करने के लिए एक अतिरिक्त इलेक्ट्रॉन की आवश्यकता है। यदि सोडियम और क्लोरीन प्रतिक्रिया करते हैं, तो सोडियम द्वारा खोया गया इलेक्ट्रॉन क्लोरीन द्वारा ग्रहण किया जा सकता है। एक इलेक्ट्रॉन प्राप्त करने के बाद, क्लोरीन परमाणु को एक इकाई नकारात्मक आवेश मिलता है, क्योंकि इसके नाभिक में 17 प्रोटॉन हैं और इसके K, L और M शेलों में कुल 18 इलेक्ट्रॉन हो जाते हैं। यह हमें क्लोराइड ऋणायन Cl⁻ देता है। इसलिए ये दोनों तत्व एक दान-स्वीकार संबंध बना सकते हैं जैसा कि नीचे दिखाया गया है (अंजीर. 3.5)। Table 3.3 कुछ तत्वों का इलेक्ट्रॉनिक विन्यास दिखाता है।
| प्रकार का तत्व | तत्व | परमाणु संख्या | इलेक्ट्रॉनों की संख्या कोश में | | | | | : - - - : | : - - - : | : - - - : | : - - - : | : - - - : | : - - - : | : - - - : | | | | | $\mathbf{K}$ | $\mathbf{L}$ | $\mathbf{M}$ | $\mathbf{N}$ | | उत्कृष्ट गैसें | हीलियम (He) | 2 | 2 | | | | | | नियॉन (Ne) | 10 | 2 | 8 | | | | | आर्गन (Ar) | 18 | 2 | 8 | 8 | | | धातु | सोडियम (Na) | 11 | 2 | 8 | 1 | | | | मैग्नीशियम (Mg) | 12 | 2 | 8 | 2 | | | | एल्यूमिनियम (Al) | 13 | 2 | 8 | 3 | | | | पोटैशियम (K) | 19 | 2 | 8 | 8 | 1 | | | कैल्शियम (Ca) | 20 | 2 | 8 | 8 | 2 | | गैर-धातु | नाइट्रोजन (N) | 7 | 2 | 5 | | | | | ऑक्सीजन (O) | 8 | 2 | 6 | | | | | फ्लोरीन (F) | 9 | 2 | 7 | | | | | फॉस्फोरस (P) | 15 | 2 | 8 | 5 | | | | गंधक (S) | 16 | 2 | 8 | 6 | | | | क्लोरीन (Cl) | 17 | 2 | 8 | 7 | |
 चित्र 3.5 सोडियम क्लोराइड की संरचना: सोडियम और क्लोराइड आयन, विपरीत आवेशों के कारण एक-दूसरे को आकर्षित करते हैं और मजबूत स्थिरवैद्युत आकर्षण बलों द्वारा एक साथ बने रहते हैं, जैसे सोडियम क्लोराइड $(NaCl)$ में। यह ध्यान देने योग्य है कि सोडियम क्लोराइल अणु के रूप में नहीं होता है, बल्कि विपरीत आवेशित आयनों का एक समूह होता है। आइए हम एक और आयनिक यौगिक, मैग्नीशियम क्लोराइड की संरचना देखें (चित्र 3.6)।
चित्र 3.5 सोडियम क्लोराइड की संरचना: सोडियम और क्लोराइड आयन, विपरीत आवेशों के कारण एक-दूसरे को आकर्षित करते हैं और मजबूत स्थिरवैद्युत आकर्षण बलों द्वारा एक साथ बने रहते हैं, जैसे सोडियम क्लोराइड $(NaCl)$ में। यह ध्यान देने योग्य है कि सोडियम क्लोराइल अणु के रूप में नहीं होता है, बल्कि विपरीत आवेशित आयनों का एक समूह होता है। आइए हम एक और आयनिक यौगिक, मैग्नीशियम क्लोराइड की संरचना देखें (चित्र 3.6)।  चित्र 3.6 मैग्नीशियम क्लोराइड की संरचना
चित्र 3.6 मैग्नीशियम क्लोराइड की संरचना
यह यौगिक इस प्रकार बनाया गया है कि एक धातु से इलेक्ट्रॉन स्थानांतरित होकर एक गैर-धातु से जुड़ता है, जिसे आयनिक यौगिक या विद्युत आबंधी यौगिक कहा जाता है। क्या आप $MgCl_2$ में उपस्थित धनायन और ऋणायन का नाम बता सकते हैं?
3.3.1 आयनिक यौगिकों के गुणधर्मों के बारे में जानने के लिए आइए निम्नलिखित गतिविधि करते हैं:
गतिविधि 3.13
- विज्ञान प्रयोगशाला में सोडियम क्लोराइड, पोटैशियम आयोडाइड, बेरियम क्लोराइड या किसी अन्य नमक का नमूना लें।
- इन लवणों का भौतिक राज्य क्या है?
- धातु के रोलर पर थोड़ी मात्रा में नमूना लें और सीधे आग में गरम करें (चित्र 3.7)। इसी प्रक्रिया को अन्य नमूनों के साथ दोहराएं।
- आपने क्या निरीक्षण किया? क्या इन नमूनों ने लौ को कोई रंग दिया? क्या ये यौगिक पिघल गए?
- इन नमूनों को पानी, पेट्रोल और मिट्टी के तेल में घोलने की कोशिश करें। क्या वे घुलते हैं?
- चित्र 3.8 में दिखाए गए अनुसार एक परिपथ बनाएं और नमक के विलयन में इलेक्ट्रोड डालें। आपने क्या निरीक्षण किया? इसी तरीके से अन्य नमक नमूनों की भी जांच करें।
- इन यौगिकों की प्रकृति के बारे में आपका क्या निष्कर्ष है?
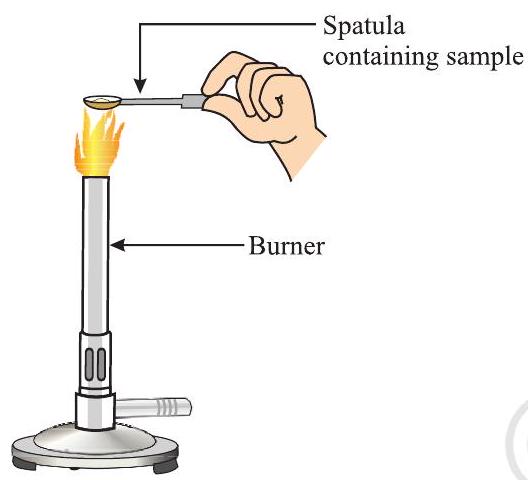
चित्र 3.7 रोलर पर नमक नमूना गरम करना
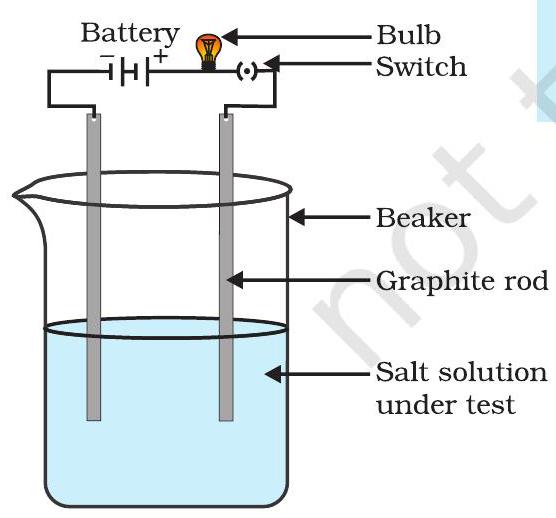 चित्र 3.8: चालकता परीक्षण - यह एक नमक का विलयन है। सारणी 3.4: कुछ आयनिक यौगिकों के गलन और क्वथनांक। एकपदीय यौगिक | गलन बिंदु (K) | क्वथनांद (K) | |:—|:—|:—| | NaCl | 1074 | 1686 | | LiCl | 887 | 1600 | | CaCl₂ | 1045 | 1900 | | CaO | 2850 | 3120 | | MgCl₂ | 981 | 1685 | आपने देखा होगा कि आयनिक यौगिकों के निम्नलिखित सामान्य गुणधर्म होते हैं: (i) भौतिक प्रकृति: आयनिक यौगिक ठोस होते हैं और कुछ हद तक कठोर होते हैं, क्योंकि इनके धनात्मक और ऋणात्मक आयनों के बीच प्रबल आकर्षण बल होता है। ये यौगिक आमतौर पर भंगुर होते हैं और दबाव लगाने पर टुकड़ों में टूट जाते हैं।
चित्र 3.8: चालकता परीक्षण - यह एक नमक का विलयन है। सारणी 3.4: कुछ आयनिक यौगिकों के गलन और क्वथनांक। एकपदीय यौगिक | गलन बिंदु (K) | क्वथनांद (K) | |:—|:—|:—| | NaCl | 1074 | 1686 | | LiCl | 887 | 1600 | | CaCl₂ | 1045 | 1900 | | CaO | 2850 | 3120 | | MgCl₂ | 981 | 1685 | आपने देखा होगा कि आयनिक यौगिकों के निम्नलिखित सामान्य गुणधर्म होते हैं: (i) भौतिक प्रकृति: आयनिक यौगिक ठोस होते हैं और कुछ हद तक कठोर होते हैं, क्योंकि इनके धनात्मक और ऋणात्मक आयनों के बीच प्रबल आकर्षण बल होता है। ये यौगिक आमतौर पर भंगुर होते हैं और दबाव लगाने पर टुकड़ों में टूट जाते हैं।
(i) गलन और क्वथनांक: आयनिक यौगिकों के गलन और क्वथनांक उच्च होते हैं (देखें Table 3.4)। ऐसा इसलिए है क्योंकि इनके मजबूत इंटर-आयनिक आकर्षण को तोड़ने के लिए काफी मात्रा में ऊर्जा की आवश्यकता होती है। (iii) विलेयता: विद्युत आबंधी यौगिक आमतौर पर पानी में विलेय होते हैं और ऐसे विलायकों में अविलेय होते हैं जैसे मिट्टी का तेल, पेट्रोल आदि।
(चतुर्थ) विद्युत् संचरण: यह विद्युत् संचरण के माध्यम से घोल में आवेशित कणों की गति को शामिल करता है। इस घोल में एक आयनिक यौगिक जल में विले आयन होते हैं, जो विद्युत् प्रवाहित होने पर विपरीत इलेक्ट्रोड की ओर गतिशील होते हैं। आयनिक यौगिक ठोस अवस्था में विद्युत् का संचरण नहीं करता, क्योंकि ठोस में आयनों की गति उनकी कठोर संरचना के कारण संभव नहीं है। परन्तु आयनिक यौगिक गलित अवस्था में विद्युत् का संचरण करता है। गलित अवस्था में यह संभव होता है क्योंकि विपरीत दिशा में आवेशित आयनों के बीच स्थिरवैद्युत् आकर्षण बल को गर्मी के कारण परास्त किया जाता है। इस प्रकार आयन स्वतंत्र रूप से गतिशील होकर विद्युत् का संचरण करते हैं। [[Sc_marker_2]]### 3.4 धातु की घटना
यह पृथ्वी की भूपर्पटी है जो धातुओं का प्रमुख स्रोत है। समुद्री जल में कुछ विलेय लवण जैसे सोडियम क्लोराइड, मैग्नीशियम क्लोराइड आदि शामिल होते हैं। वे तत्व या यौगिक जो पृथ्वी की भूपर्पटी में स्वाभाविक रूप से घटित होते हैं, खनिज के रूप में जाने जाते हैं। पर कुछ स्थानों पर खनिज में किसी विशेष धातु का प्रतिशत बहुत अधिक होता है और यह धातु लाभप्रद रूप से निकाली जा सकती है। ऐसे खनिजों को अयस्क कहा जाता है।
तुमने सीखा है कि यह प्रतिक्रियाशीलता श्रृंखला धातुओं के बारे में है। यह ज्ञान होने से तुम आसानी से समझ सकते हो कि किसी धातु को उसके अयस्क से कैसे निकाला गया है। कुछ धातुएँ पृथ्वी की भूपर्पटी में मुक्त अवस्था में मिलती हैं। कुछ उनके यौगिकों के रूप में मिलती हैं। जो धातुएँ प्रतिक्रियाशीलता श्रृंखला में नीचे हैं, वे न्यूनतम प्रतिक्रियाशील होती हैं और अक्सर मुक्त अवस्था में मिलती हैं। उदाहरण के लिए, सोना, चांदी, प्लैटिनम और तांबा मुक्त अवस्था में मिलते हैं। तांबा और चांदी संयुक्त अवस्था में भी मिलते हैं, जैसे उनके सल्फाइड या ऑक्साइड अयस्क। जो धातुएँ प्रतिक्रियाशीलता श्रृंखला के शीर्ष पर हैं ($K, Na, Ca, Mg$ और $Al$), वे अत्यंत प्रतिक्रियाशील होती हैं और कभी भी प्रकृति में मुक्त तत्व के रूप में नहीं मिलती हैं। जो धातुएँ प्रतिक्रियाशीलता श्रृंखला के मध्य में हैं ($Zn, Fe, Pb$ आदि), वे मध्यम प्रतिक्रियाशील होती हैं और पृथ्वी की भूपर्पटी में मुख्यतः ऑक्साइड्स, सल्फाइड्स या कार्बोनेट्स के रूप में मिलती हैं। तुम पाओगे कि अधिकांश धातुओं के अयस्क ऑक्साइड होते हैं। ऐसा इसलिए है क्योंकि ऑक्सीजन एक अत्यंत प्रतिक्रियाशील तत्व है और पृथ्वी पर बहुत प्रचुर मात्रा में है।
इस प्रकार, धातु की प्रतिक्रियाशीलता के आधार पर हम धातुओं को निम्नलिखित तीन श्रेणियों में बाँट सकते हैं (अंजीर. 3.9) - (i) धातु की निम्न प्रतिक्रियाशीलता; (ii) धातु की मध्यम प्रतिक्रियाशीलता; (iii) धातु की उच्च प्रतिक्रियाशीलता। विभिन्न तकनीकों का उपयोग किया जाता है प्रत्येक श्रेणी की धातुओं को प्राप्त करने के लिए। 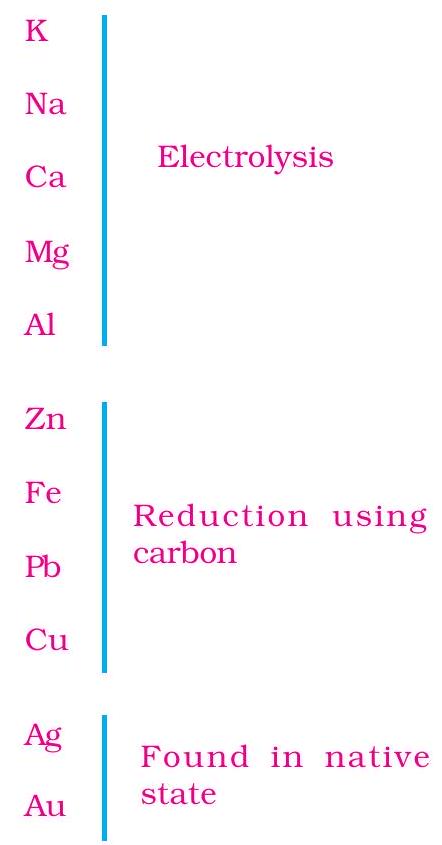 चित्र 3.9 गतिविधि श्रृंखला और संबंधित धातुकर्म अयस्क से शुद्ध धातु के निष्कर्षण में कई चरण शामिल होते हैं। इन चरणों का सारांश अंजीर. 3.10 में दिया गया है। प्रत्येक चरण को निम्नलिखित अनुभाग में विस्तार से समझाया गया है।
चित्र 3.9 गतिविधि श्रृंखला और संबंधित धातुकर्म अयस्क से शुद्ध धातु के निष्कर्षण में कई चरण शामिल होते हैं। इन चरणों का सारांश अंजीर. 3.10 में दिया गया है। प्रत्येक चरण को निम्नलिखित अनुभाग में विस्तार से समझाया गया है। 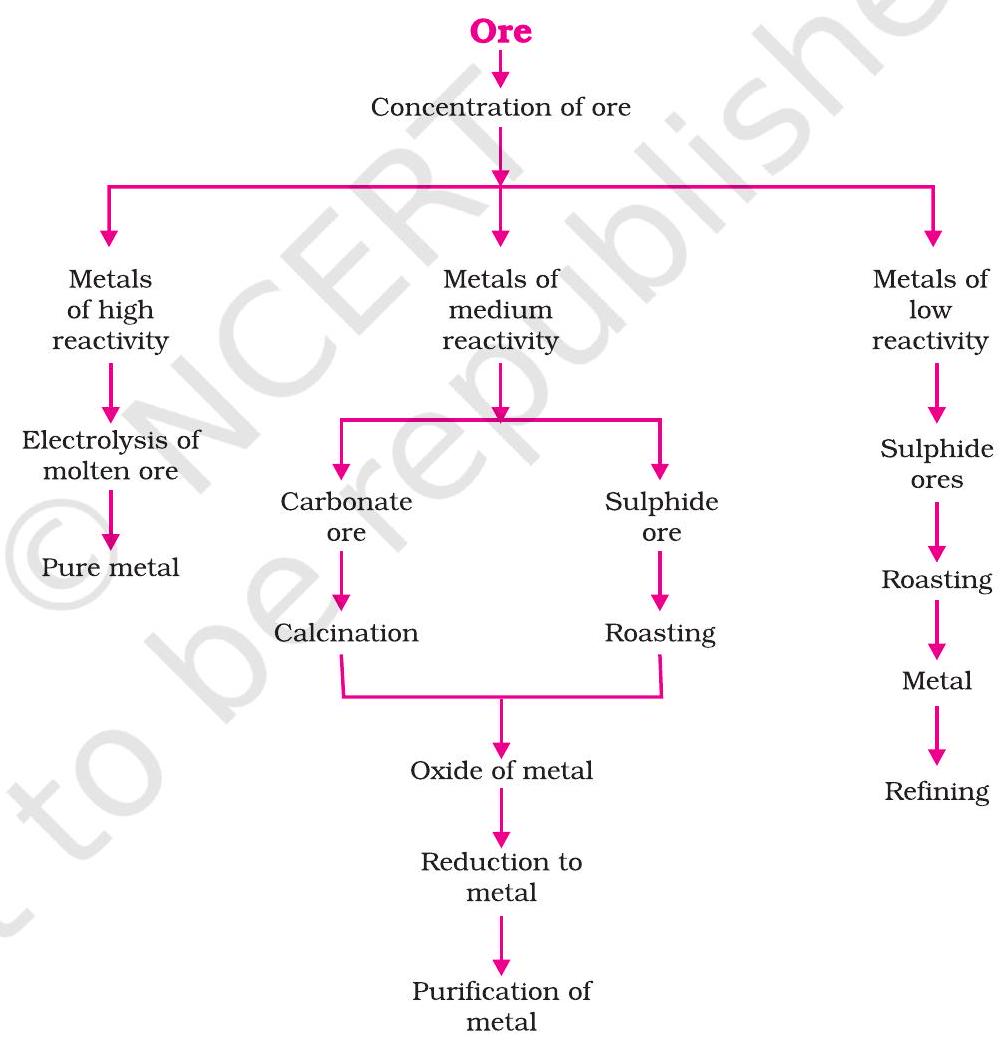
आकृति 3.10 चरण संलग्न में यह निष्कर्षण धातु से अयस्क का है।
3.4.2 समृद्धि का अयस्क अयस्क खनिज से यह धात्त्विक पदार्थ होता है, जो आमतौर पर मिट्टी, रेत आदि जैसी बड़ी मात्रा में अशुद्धियों से दूषित होता है, जिसे गैंग कहा जाता है। इन अशुद्धियों को अयस्क से हटाना आवश्यक होता है, इससे पहले कि धातु का निष्कर्षण किया जाए। इन प्रक्रियाओं का उपयोग अयस्क से गैंग को हटाने के लिए गैंग और अयस्क के भौतिक या रासायनिक गुणों के अंतर पर आधारित होता है। विभिन्न पृथक्करण तकनीकें तदनुसार नियोजित की जाती हैं।
3.4.3 धातु का निकालना निम्न गतिविधि श्रृंखला वाली धातुएं बहुत अक्रिय होती हैं। इन धातुओं के ऑक्साइड्स को धातु में परिवर्तित करने के लिए केवल गरम करना पर्याप्त होता है। उदाहरण के लिए, सिंदूर (HgS) पारा का एक अयस्क है। जब इसे वायु में गरम किया जाता है, तो यह पहले पारदीय ऑक्साइड (HgO) में रूपांतरित होता है। फिर पारदीय ऑक्साइड को आगे गरम करने पर यह पारा में कम हो जाता है।
$$\begin{aligned} & 2 \text{Hgs} (s) + 3 \text{O}_2 (g) \xrightarrow{\text{गर्मी}} 2 \text{HgO} (s) + 2 \text{SO}_2 (g) \ & 2 \text{HgO} (s) \xrightarrow{\text{गर्मी}} 2 \text{Hg} (l) + \text{O}_2 (g) \end{aligned}$$
इसी प्रकार, तांबा जो कि प्रकृति में (\text{Cu}_2\text{S}) के रूप में पाया जाता है, उसे इसके अयस्क से केवल गर्म करने और वायु द्वारा प्राप्त किया जाता है।
$$\begin{aligned} & 2 \text{Cu}_2\text{S} + 3 \text{O}_2 (g) \xrightarrow{\text{गर्मी}} 2 \text{Cu}_2\text{O} (s) + 2 \text{SO}_2 (g) \ & 2 \text{Cu}_2\text{O} + \text{Cu}_2\text{S} \xrightarrow{\text{गर्मी}} 6 \text{Cu} (s) + \text{SO}_2 (g) \end{aligned}$$
3.4.4 निकालना धातु में यह मध्य की गतिविधि श्रृंखला
यह धातुओं की मध्यम गतिविधि श्रृंखला में लोहा, जिंक, सीसा, तांबा आदि मध्यम प्रतिक्रियाशील धातुएँ आती हैं। ये सामान्यतः प्रकृति में सल्फाइड्स या कार्बोनेट्स के रूप में पाई जाती हैं। इन धातुओं के ऑक्साइड्स को इनके सल्फाइड्स और कार्बोनेट्स की तुलना में आसानी से प्राप्त किया जा सकता है। इसलिए, पूर्व-कलन के लिए, इन धातुओं के सल्फाइड्स और कार्बोनेट्स को धातु ऑक्साइड्स में रूपांतरित करना आवश्यक होता है।
सल्फाइड अयस्कों को अतिरिक्त वायु की उपस्थिति में तेज़ी से गरम करके ऑक्साइड्स में रूपांतरित किया जाता है। इस प्रक्रिया को भुना हुआ कहा जाता है। कार्बोनेट अयस्कों को सीमित वायु में गरम करके ऑक्साइड्स में बदला जाता है। इस प्रक्रिया को दहन कहा जाता है।
भुना हुआ और दहन के दौरान होने वाली रासायनिक प्रतिक्रियाओं को जिंक अयस्क के उदाहरण से इस प्रकार दिखाया गया है -
भुना हुआ: $$ 2 \ \mathrm { Zns } ( \ \mathrm { s } ) + 3 \ \mathrm { O } _ { 2 } ( \ \mathrm { ~ g } ) \ xrightarrow { \ पाठ { गर्मी } } 2 \ \mathrm { ज़ेडएनओ } ( \ \mathrm { s } ) + 2 \ \mathrm { इसलिए } _ { 2 } ( \ \mathrm { ~ g } ) $$
दहन: $$\ \mathrm{ZnCO_3}(s) \xrightarrow{\text{गर्मी}} \ \mathrm{ZnO}(s) + \mathrm{CO_2}(g)$$ ये धातु ऑक्साइड्स हैं। इन्हें संगत धातु में परिवर्तित करने के लिए उपयुक्त अपचायक एजेंट्स जैसे कार्बन का उपयोग किया जाता है। उदाहरण के लिए, जब जिंक ऑक्साइड को कार्बन के साथ गरम किया जाता है, तो यह धात्विक जिंक में अपचयित हो जाता है: $$\mathrm{ZnO}(s) + C(s) \rightarrow \mathrm{Zn}(s) + \mathrm{CO}(g)$$ आप पहले से ही इस प्रक्रिया को ऑक्सीकरण और अपचय के रूप में पहले अध्याय में समझ चुके हैं। धातु के यौगिकों से धातु प्राप्त करना भी एक अपचय प्रक्रिया है। कार्बन (कोक) के अतिरिक्त, कभी-कभी विस्थापन प्रतिक्रियाओं का भी उपयोग किया जाता है। अत्यधिक प्रतिक्रियाशील धातुएँ जैसे सोडियम, कैल्शियम, एल्यूमिनियम आदि को अपचायक एजेंट्स के रूप में उपयोग किया जाता है क्योंकि वे कम प्रतिक्रियाशील धातुओं को उनके यौगिकों से विस्थापित कर सकते हैं। उदाहरण के लिए, जब मैंगनीज डाइऑक्साइड को एल्यूमिनियम पाउडर के साथ गरम किया जाता है, तो निम्नलिखित प्रतिक्रिया होती है: $$3\mathrm{MnO_2}(s) + 4\mathrm{Al}(s) \rightarrow 3\mathrm{Mn}(l) + 2\mathrm{Al_2O_3}(s) + \text{गर्मी}$$
 चित्र 3.11 थर्मिट प्रक्रिया
चित्र 3.11 थर्मिट प्रक्रिया
क्या आप पहचान सकते हैं कि रेलवे पटरियों को जोड़ने के लिए उपयोग होने वाले पदार्थ कौन-से हैं और ये कैसे प्राप्त किए जाते हैं? ये विस्थापन प्रतिक्रियाएँ अत्यधिक उष्माक्षेपी होती हैं। इस प्रक्रिया में इतनी अधिक ऊष्मा उत्पन्न होती है कि धातु गलित अवस्था में आ जाती है। वास्तव में, लोहे (III) ऑक्साइड $(Fe_2O_3)$ और एल्यूमिनियम की यह प्रतिक्रिया रेलवे पटरियों या टूटे हुए मशीन भागों को जोड़ने के लिए उपयोग की जाती है। इस प्रतिक्रिया को थर्मिट प्रतिक्रिया के नाम से जाना जाता है।
$Fe_2O_3(s) + 2Al(s) \rightarrow 2Fe(l) + Al_2O_3(s) + \text{ऊष्मा}$
3.4.5 धातु की ओर यह शीर्ष की गतिविधि श्रृंखला
यह धातुएँ ऊपर की ओर प्रतिक्रियाशीलता श्रृंखला में बहुत अधिक प्रतिक्रियाशील होती हैं। इन्हें उनके यौगिकों से कार्बन को गरम करके प्राप्त नहीं किया जा सकता। उदाहरण के लिए, कार्बन सोडियम, मैग्नीशियम, कैल्शियम, एल्यूमिनियम आदि के ऑक्साइडों को कम नहीं कर सकता, क्योंकि इन धातुओं की ऑक्सीजन से अधिक समानता होती है। इन धातुओं को विद्युत अपघटनीय कमी द्वारा प्राप्त किया जाता है। उदाहरण के लिए, सोडियम, मैग्नीशियम और कैल्शियम को उनके गलित क्लोराइडों के विद्युत अपघटन द्वारा प्राप्त किया जाता है। यह धातुएँ कैथोड पर (जो नकारात्मक रूप से आवेशित इलेक्ट्रोड होता है) जमा होती हैं, जबकि क्लोरीन ऐनोड पर (जो सकारात्मक रूप से आवेशित इलेक्ट्रोड होता है) मुक्त होता है। ये प्रतिक्रियाएँ हैं - पर कैथोड $Na^{+}+e^{-} \to Na$ पर ऐनोड $\quad 2 Cl^{-} \to Cl_2+2 e^{-}$ इसी प्रकार, एल्यूमिनियम को एल्यूमिनियम ऑक्साइड के विद्युत अपघटनीय कमी द्वारा प्राप्त किया जाता है।
इस धातु को उपरोक्त विभिन्न कमी प्रक्रियाओं द्वारा उत्पन्न किया गया है, लेकिन यह बहुत शुद्ध नहीं होती। इनमें अशुद्धियाँ होती हैं, जिन्हें हटाकर शुद्ध धातु प्राप्त करनी होती है। अशुद्ध धातु को परिष्कृत करने की सबसे व्यापक रूप से प्रयुक्त विधि विद्युत अपघटनीय परिष्करण है। 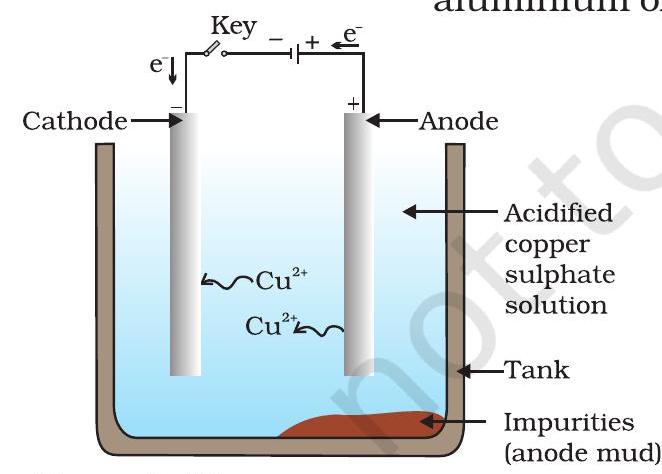 चित्र 3.12 तांबे का विद्युत अपघटनीय परिष्करण। यह विद्युतअपघट्य एक अम्लीयकृत तांबा सल्फेट विलयन है। इसका ऐनोड अशुद्ध तांबा है, जबकि कैथोड शुद्ध तांबे की एक पत्ती है। विद्युत धारा प्रवाहित होने पर शुद्ध तांबा कैथोड पर जमा होता है।
चित्र 3.12 तांबे का विद्युत अपघटनीय परिष्करण। यह विद्युतअपघट्य एक अम्लीयकृत तांबा सल्फेट विलयन है। इसका ऐनोड अशुद्ध तांबा है, जबकि कैथोड शुद्ध तांबे की एक पत्ती है। विद्युत धारा प्रवाहित होने पर शुद्ध तांबा कैथोड पर जमा होता है।
विद्युत अपघटनीय परिष्करण: बहुत-सी धातुएँ, जैसे तांबा, जिंक, टिन, निकल, चांदी, सोना आदि, विद्युत अपघटन द्वारा परिष्कृत की जाती हैं। इस प्रक्रिया में अशुद्ध धातु को ऐनोड बनाया जाता है और पतली चादर के रूप में शुद्ध धातु को कैथोड बनाया जाता है। धातु के लवण का विलयन विद्युतअपघट्य के रूप में उपयोग किया जाता है। यह उपकरण अंजीर 3.12 में दिखाए अनुसार एक सेल में एकत्रित किया जाता है। जब विद्युतअपघट्य से धारा प्रवाहित होती है, तो ऐनोड से शुद्ध धातु विलयन में घुल जाती है। विलयन से समतुल्य मात्रा में शुद्ध धातु कैथोड पर जमा हो जाती है। विलेय अशुद्धियाँ विलयन में चली जाती हैं, जबकि अविलेय अशुद्धियाँ ऐनोड के नीचे तल पर बस जाती हैं और ऐनोड कीचड़ के रूप में जानी जाती हैं। [[Sc_marker_3]] ### 3.5 संक्षारण आपने अध्याय 1 में संक्षारण के बारे में निम्नलिखित सीखा है -
चांदी लेख बन जाता है काला बाद में कुछ समय जब अनावृत होकर वायु से संपर्क में आता है। यह इसलिए होता है क्योंकि यह प्रतिक्रिया करता है वायु में मौजूद गंधक के साथ और बनाता है चांदी सल्फाइड की एक परत। तांबा प्रतिक्रिया करता है नम वायु में मौजूद कार्बन डाइऑक्साइड के साथ और धीरे-धीरे खो देता है अपनी चमकदार भूरी सतह और प्राप्त करता है एक हरी परत। यह हरा पदार्थ होता है मूल रूप से तांबा कार्बोनेट। लोहा जब अनावृत रहता है नम वायु में लंबे समय तक तो प्राप्त करता है एक भूरी झरझरा पदार्थ की परत जिसे कहा जाता है जंग। आइए हम खोजें कि किन परिस्थितियों में लोहा जंग लगता है।
गतिविधि 3.15
- तीन परीक्षण नलिकाएँ लें और प्रत्येक में साफ लोहे का एक नाखून रखें।
- इन परीक्षण नलिकाओं को A, B और C लेबल करें। परीक्षण नलिका A में कुछ पानी डालें और इसे कॉर्क से बंद करें।
- परीक्षण नलिका B में उबला हुआ आसवित पानी डालें, लगभग 1 mL तेल जोड़ें और इसे कॉर्क से बंद करें। यह तेल पानी पर तैरेगा और पानी को वायु से मिलने से रोकेगा।
- परीक्षण नलिका C में कुछ अनजलित कैल्शियम क्लोराइड रखें और इसे कॉर्क से बंद करें। अनजलित कैल्शियम क्लोराइ्ड वायु से नमी को अवशोषित करेगा, यदि कोई हो। इन परीक्षण नलिकाओं को कुछ दिनों के लिए छोड़ दें और फिर निरीक्षण करें (अंजीर. 3.13)। आप देखेंगे कि परीक्षण नलिका A में लोहे का नाखून जंग लगा है, लेकिन परीक्षण नलिकाओं B और C में नाखून जंगे नहीं हैं। परीक्षण नलिका A में नाखून वायु और पानी दोनों के संपर्क में है। परीक्षण नलिका B में नाखून केवल पानी के संपर्क में है, और परीक्षण नलिका C में नाखून सूखी वायु के संपर्क में है। यह हमें क्या बताता है कि लोहा किन परिस्थितियों में जंग लगता है?
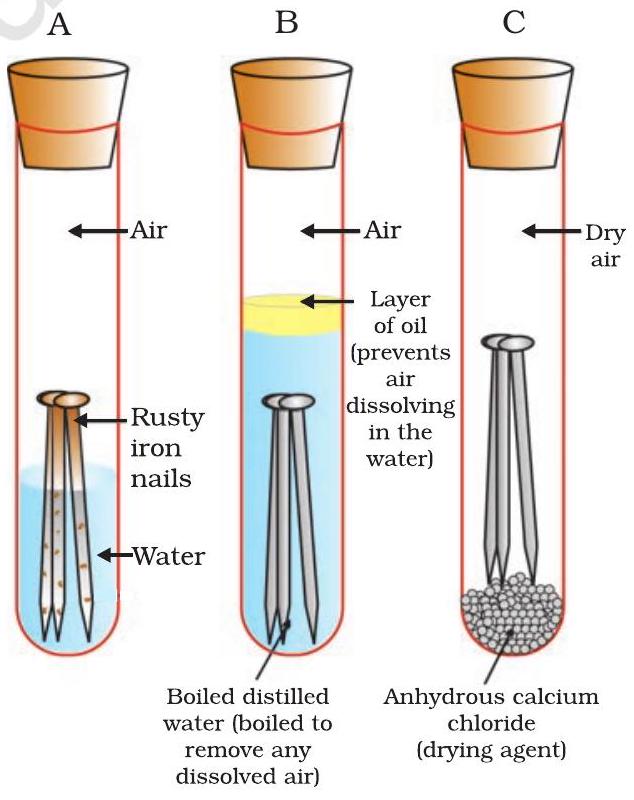 चित्र 3.13 जांचना: इन शर्तों के अंतर्गत कौन-सा लोहा जंग लगता है। नलिका A में वायु और पानी दोनों मौजूद हैं। नलिका B में पानी तो है, पर उसमें विलयित वायु नहीं है। नलिका C में वायु सूखी है। ### 3.5.1 संक्षारण की रोकथाम लोहे के जंग लगने को चित्रकला, तेल लगाना, चिकनाई, जस्ता चढ़ाना, क्रोम प्लेटिंग, ऐनोडाइज़िंग या मिश्र धातु बनाकर रोका जा सकता है। जस्ताकरण इस्पात और लोहे को जंग से बचाने की एक विधि है, जिसमें उन पर जिंक की एक पतली परत चढ़ाई जाती है। यदि जिंक कोटिंग टूट जाए तब भी जस्ता लेपित वस्तु जंग से सुरक्षित रहती है। क्या आप बता सकते हैं कि ऐसा क्यों होता है?
चित्र 3.13 जांचना: इन शर्तों के अंतर्गत कौन-सा लोहा जंग लगता है। नलिका A में वायु और पानी दोनों मौजूद हैं। नलिका B में पानी तो है, पर उसमें विलयित वायु नहीं है। नलिका C में वायु सूखी है। ### 3.5.1 संक्षारण की रोकथाम लोहे के जंग लगने को चित्रकला, तेल लगाना, चिकनाई, जस्ता चढ़ाना, क्रोम प्लेटिंग, ऐनोडाइज़िंग या मिश्र धातु बनाकर रोका जा सकता है। जस्ताकरण इस्पात और लोहे को जंग से बचाने की एक विधि है, जिसमें उन पर जिंक की एक पतली परत चढ़ाई जाती है। यदि जिंक कोटिंग टूट जाए तब भी जस्ता लेपित वस्तु जंग से सुरक्षित रहती है। क्या आप बता सकते हैं कि ऐसा क्यों होता है?
मिश्रधातु बनाना धातु के गुणधर्मों को सुधारने की एक बहुत अच्छी विधि है। हम इस विधि से वांछित गुणधर्म प्राप्त कर सकते हैं। उदाहरण के लिए, लोहा सबसे अधिक उपयोग होने वाली धातु है, लेकिन इसे कभी भी शुद्ध रूप में नहीं उपयोग किया जाता। ऐसा इसलिए है क्योंकि शुद्ध लोहा बहुत नरम होता है और गरम होने पर आसानी से फैल जाता है। लेकिन यदि इसे थोड़ी मात्रा में कार्बन (लगभग $0.05 %$) के साथ मिश्रित किया जाए, तो यह कठिन और मजबूत बन जाता है। जब लोहे को निकल और क्रोमियम के साथ मिश्रित किया जाता है, तो हम स्टेनलेस इस्पात प्राप्त करते हैं, जो कठिन होता है और जंग नहीं लगता। इस प्रकार, यदि लोहे को कुछ अन्य पदार्थों के साथ मिश्रित किया जाए, तो इसके गुणधर्म बदल जाते हैं। वास्तव में, किसी भी धातु के गुणधर्मों को बदला जा सकता है यदि उसे किसी अन्य पदार्थ के साथ मिश्रित किया जाए। यह जोड़ा गया पदार्थ धातु या अधातु हो सकता है। एक मिश्रधातु दो या अधिक धातुओं, या एक धातु और एक अधातु का एक समांगिक मिश्रण होता है। इसे प्राथमिक धातु को पहले गलाकर, फिर उसमें अन्य तत्वों को निश्चित अनुपात में मिलाकर तैयार किया जाता है। फिर इसे कमरा तापमान तक ठंडा किया जाता है।
क्या तुम जानना चाहते हो?
शुद्ध सोना, जैसे कि 24 कैरेट सोना, बहुत नरम होता है। इसलिए यह गहने बनाने के लिए उपयुक्त नहीं है। इसे कठिन बनाने के लिए इसे चांदी या तांबे जैसी धातुओं के साथ मिलाया जाता है। आमतौर पर भारत में आभूषण बनाने के लिए 22 कैरेट सोना उपयोग किया जाता है। इसका मतलब है कि इसमें 22 भाग शुद्ध सोना और 2 भाग चांदी या तांबे जैसी मिश्र धातु होती है।

दिल्ली का लोहा स्तंभ
यदि एक धातु का यह रूप है पारा, तो यह मिश्रधातु है जैसा कि एक मिश्रधातु को जाना जाता है। यह विद्युत चालकता और गलनांक में शुद्ध धातु की तुलना में कम है। उदाहरण के लिए, पीतल—तांबे और जिंक (Cu और Zn) की मिश्रधातु—और कांस्य—तांबे और टिन (Cu और Sn) की मिश्रधातु—बिजली की चालकता में तांबे जितनी अच्छी नहीं होती, जबकि तांबे का उपयोग विद्युत परिपथ बनाने में किया जाता है। सोल्डर—सीसे और टिन (Pb और Sn) की मिश्रधातु—का गलनांक कम होता है और इसका उपयोग विद्युत तारों को वेल्डिंग करने में किया जाता है।
अधिक जानने के लिए!
यह लोहे का स्तंभ, जो दिल्ली की कुतुब मीनार में है, भारतीय लोहा श्रमिकों द्वारा 1600 से अधिक वर्ष पहले बनाया गया था। उन्होंने एक ऐसी प्रक्रिया विकसित की थी जिससे लोहे को जंग लगने से रोका गया। इसके जंग-प्रतिरोधी गुणों की जांच दुनिया भर के वैज्ञानिकों द्वारा की गई है। यह लोहे का स्तंभ 8 मीटर ऊँचा है और इसका वजन 6 टन (6000 किग्रा) है।
क्या तुमने सीखा
तत्वों को धातु और गैर-धातु में वर्गीकृत किया जाता है। धातुएँ चमकदार, नम्य, तन्य और गर्मी-बिजली की अच्छी चालक होती हैं। वे कमरे के तापमान पर ठोस होती हैं, सिवाय पारा के जो द्रव है। धातु गैर-धातु से इलेक्ट्रॉन खोकर सकारात्मक आयन बनाती है। धातुएँ ऑक्सीजन से मिलकर बुनियादी ऑक्साइड बनाती हैं। एल्यूमिनियम ऑक्साइड और जिंक ऑक्साइड यह गुणधर्म दिखाते हैं कि वे बुनियादी के साथ-साथ अम्लीय ऑक्साइड भी हैं। इन्हें उभयधर्मी ऑक्साइड कहा जाता है। विभिन्न धातुओं की पानी और तनु अम्ल के प्रति भिन्न-भिन्न प्रतिक्रियाशीलताएँ होती हैं। सामान्य धातुओं की एक सूची जिन्हें उनकी घटती प्रतिक्रियाशीलता के क्रम में व्यवस्थित किया गया है, गतिविधि श्रृंखला कहलाती है। गतिविधि श्रृंखला में हाइड्रोजन से ऊपर स्थित धातु तनु अम्ल से हाइड्रोजन को विस्थापित कर सकती है। अधिक प्रतिक्रियाशील धातु कम प्रतिक्रियाशील धातु के लवण विलय से उसे विस्थापित कर देती है। धातु प्रकृति में मुक्त तत्व के रूप में या अपने यौगिकों के रूप में पाई जाती है। धातु को उसके अयस्क से निकालना और फिर उसे उपयोग के लिए परिष्कृत करना धातुकर्म कहलाता है। एक मिश्रधातु दो या अधिक धातुओं, या एक धातु और एक गैर-धातु का समांगी मिश्रण होता है। कुछ धातुओं, जैसे लोहे की सतह, जब वे लंबे समय तक नम वायु से अनावृत रहती हैं, तो संक्षारित हो जाती हैं; इसे संक्षारण कहते हैं। गैर-धातुओं के गुणधर्म धातुओं से विपरीत होते हैं। वे न तो नम्य होती हैं और न ही तन्य। वे गर्मी और बिजली की खराब चालक होती हैं, सिवाय ग्रेफाइट के जो बिजली का संचालन करता है। गैर-धातु धातु से प्रतिक्रिया करते समय इलेक्ट्रॉन ग्रहण करके ऋणावेशित आयन बनाते हैं। गैर-धातु अम्लीय या तटस्थ ऑक्साइड बनाते हैं। गैर-धातु तनु अम्ल से हाइड्रोजन को विस्थापित नहीं करते; वे हाइड्रोजन से मिलकर हाइड्राइड बनाते हैं।
मैंने अपने जीवन में पहली बार किसी को इस तरह से चाहा है। तुम्हारी मुस्कान, तुम्हारी आँखें, तुम्हारी हँ



